Ученые записки Крымского федерального университета имени В. И. Вернадского
Биология. Химия. Том 11 (77). 2025. № 2. С. 333–343.
УДК 547.918:543.42:615.074
DOI 10.29039/2413-1725-2025-11-2-333-343
БИЯДЕРНЫЕ КОМПЛЕКСЫ МЕДИ(II) НА ОСНОВЕ СПЕЙСЕРИРОВАННЫХ ОКСИГИДРАЗОНОВЫХ КИСЛОТ
Гончарук Д. Е., Шульгин В. Ф., Гусев А. Н.
Институт биохимических технологий, экологии и фармации (структурное подразделение) ФГАОУ ВО «Крымский федеральный университет им. В. И. Вернадского», Симферополь, Россия
Е-mail: goncharykd0@gmail.com
Получены биядерные комплексы меди(II) со спейсерированными ацилдигидразонами кислот. Сольватный состав комплексов [Cu2L3(py)2]∙6H2O и [Cu2L4(py)2]∙6H2O был подтвержден с помощью термогравиметрического и элементного анализа. Для исследования способа координации лигандов были записаны ИК-спектры полученных комплексов. В спектрах ЭПР синтезированных комплексов наблюдается слабо разрешенная сверхтонкая структура с константой порядка 30 Гс, характерная для димеров меди(II) со слабым обменным взаимодействием между ядрами металла.
Ключевые слова: биядерные комплексы меди(II), ИК-спектры, электронный парамагнитный резонанс, сверхтонкая структура, обменное взаимодействие.
ВВЕДЕНИЕ
Наиболее интересную группу полиядерных комплексов составляют биядерные соединения, проявляющие необычные магнитные свойства, которые не сводятся к магнетизму, характерному для моноядерных соединений или диамагнетизму, типичному для кластеров с прочными связями металл–металл [1]. Причиной данных магнитных свойств является так называемые обменные взаимодействия – квантовые эффекты, вызывающие коррелированное поведение спинов неспаренных электронов. Характер спин-спиновых взаимодействий в димерах и обменных кластерах зависит от деталей геометрического и электронного строения соединений и определяющим образом влияет на их магнитные свойства.
При изучении слабых взаимодействий довольно продуктивным является использование методов спектроскопии ЭПР. Особо удобен этот метод при изучении димерных комплексов меди(II) [2–4]. В последнее время повышенный интерес вызывают координационные соединения, у которых реализуются обменные взаимодействия между ионами металла, разделенными расстоянием более 3 Ǻ, характерном для большинства обменных димеров. В литературе описано большое количество обменных димеров, тогда как данные о комплексах с расстоянием между парамагнитными ионами более 3 Ǻ ограничены [5–7].
В настоящей работе рассматриваются спейсерированные оксигидразоновые кислоты в качестве потенциальных лигандов, в которых можно отметить некоторые особенности в структуре и возможность плавно изменять расстояние между катионами меди(II), а также полученные биядерные комплексы меди(II) на основе спейсерированных ацилгидразонов некоторых дикарбоновых кислот.
МАТЕРИАЛЫ И МЕТОДЫ
Получение пропан-1,3- и бутан-1,4-бис(N-2-тозиламино-бензилиденоксигидразоновой кислоты) (H4L3 и H4L4 соответственно).
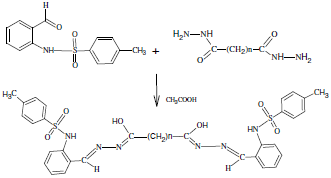
К раствору гидразида глутаровой или адипиновой кислоты (0,005 моль) в 50 мл этанола добавили раствор 2,6 г 2-(N-тозиламино)бензальдегида (0,0095 моль) в 20 мл хлороформа. Затем при перемешивании добавили 5 капель ледяной уксусной кислоты. Полученную смесь кипятили в течение 30 минут при перемешивании и оставили на ночь. Выпавший осадок отфильтровали, промыли небольшим количеством этилового спирта и высушили на воздухе (рис. 1).
Рис. 1. Схема синтеза алкалиден-бис(N-2-тозиламинобензилиден-оксигидразоновой кислоты) (H4L3 и H4L4 соответственно, n = 3, 4).
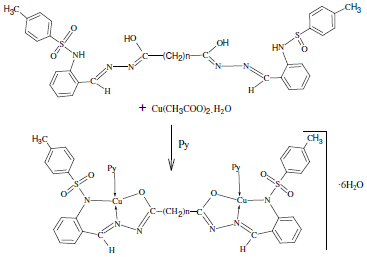
Синтез биядерного комплекса меди(II) состава [Cu2L3(py)2]∙6H2O (комплекс 1) и [Cu2L4(py)2]∙6H2O (комплекс 2). К раствору лиганда H4L3 или H4L4 (0,001 моль) в 20 мл метилового спирта добавили 0,4 г ацетата меди(II) (0,002 моль) при нагревании и перемешивании. Затем добавили 1 мл пиридина, кипятили и перемешивали в течение 40 минут. Полученную смесь оставили на ночь. Выпавший осадок отфильтровали, промыли небольшим количеством метилового спирта и высушили на воздухе (рис. 2).
ИК-спектры поглощения записаны на ИК-спектрометре с Фурье-преобразованием Spectrum Two, снабженном приставкой однократно нарушенного полного внутреннего отражения (Perkin-Elmer). Элементный анализ выполняли на автоматическом анализаторе EUROVector 3000A. Спектры электронного парамагнитного резонанса записаны на спектрометре SPINSCANX в X диапазоне. Термогравиметрический анализ выполняли на синхронном термическом анализаторе STA 6000(Perkin-Elmer).
Рис. 2. Схема синтеза комплекса 1 и 2 (n=3, 4).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Исследуемые координационные соединения получены взаимодействием ацетата меди(II) со спейсерированными ацилгидразонами кислот в метаноле в присутствии пиридина. Реакция идет с депротонизацией енольной формы лиганда и аминного атома азота и ведет к образованию комплексов [Cu2L].
Количественный состав комплексов подтвержден данными элементного анализа. Данные элементного анализа полученных комплексов представлены в таблице 1.
Таблица 1
Данные элементного анализа комплексов 1 и 2
| Данные элементного анализа | ||||||
| Соединение и его брутто-формула | Найдено, % | Вычислено, % | ||||
| С | Н | N | С | Н | N | |
| [Cu2L3(py)2]∙6H2O (комплекс 1) C43H40N8S2O6Cu2 | 48,51 | 4,89 | 10,40 | 48,50 | 4,92 | 10,52 |
| [Cu2L4(py)2]∙6H2O (комплекс 2) C44H42N8S2O6Cu2 | 48,94 | 5,25 | 10,45 | 48,98 | 5,04 | 10,39 |
Сольватный состав комплексов 1 и 2 был подтвержден с помощью термогравиметрического анализа. На рисунках 3 и 4 представлены термограммы исследуемых комплексов.
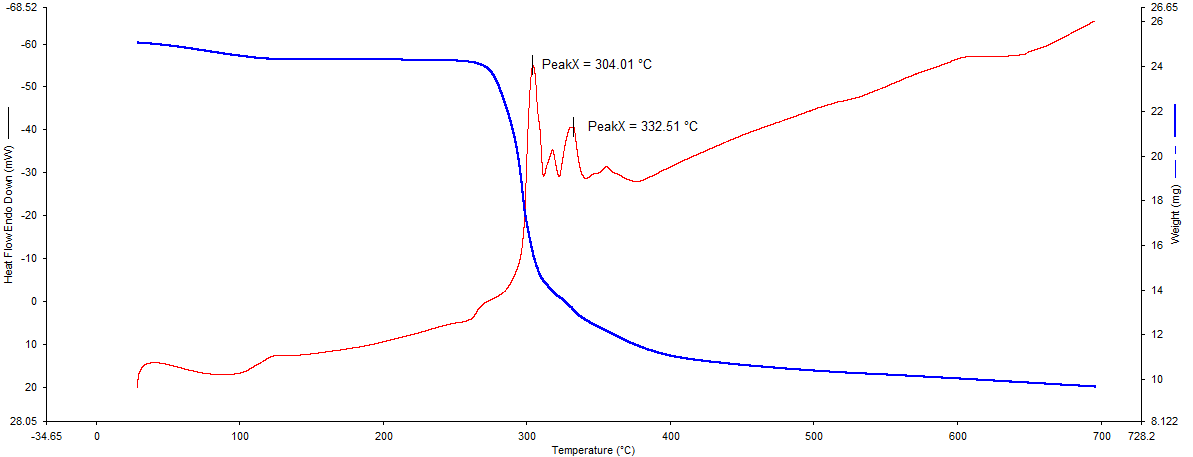
Рис. 3. Термограмма комплекса 1.
По термограмме исследуемого комплекса установлено, что комплекс 1 устойчив до 48 °С, далее происходит удаление шести внешнесферных молекул воды, потеря массы составляет 10,2 %. Процесс заканчивается при 122 °С и сопровождается небольшим эндотермическим эффектом с минимумом при 101 °С. При 260 °С начинается термическое разложение комплекса. Процесс заканчивается при 380 °С и сопровождается двумя экзотермическими эффектами с максимумами при 304 °С и 332 °С. Окончательная потеря массы образца равна 61,2 %.
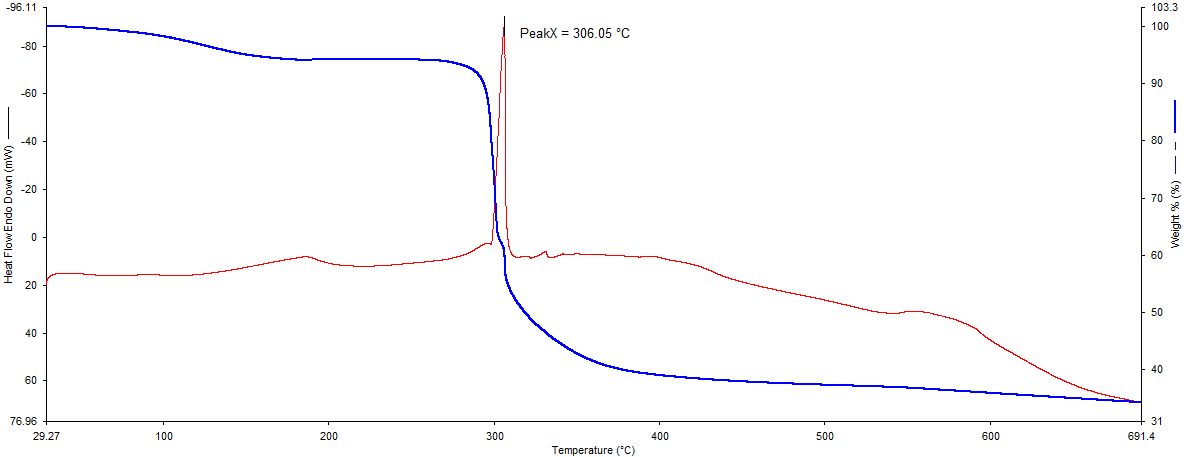
Рис. 4. Термограмма комплекса 2.
По термограмме комплекса 2 установлено, что соединение устойчиво до 110 °С, далее происходит удаление шести внешнесферных молекул воды, потеря массы составляет 10 %. Процесс заканчивается при 203 °С и сопровождается небольшим экзотермическим эффектом с максимумом при 189 °С. При 271 °С начинается термическое разложение комплекса. Процесс заканчивается при 388 °С и сопровождается мощным экзотермическим эффектом, напоминающий взрыв с максимумом при 306 °С. Окончательная потеря массы образца равна 65,3 %.
Способ координации определялся на основании данных полученных спектров исследуемых комплексов, а также соответствующих лигандов. Для подтверждения качественного состава полученных лигандов, были записаны соответствующие ИК-спектры.
ИК-спектры лигандов H4L3 и H4L4 представлены на рисунках 5 и 6.
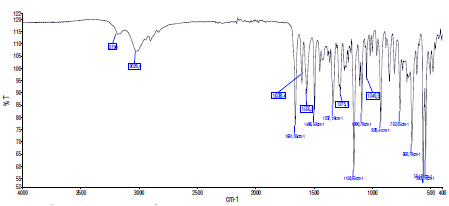
Рис. 5. ИК-спектр пропан-1,3-бис(N-2-тозиламинобензилиден-оксигидразоновой кислоты) (H4L3).
В ИК-спектре лиганда H4L3 наблюдается ряд полос поглощения, среди которых следует выделить: ν(OH) – 3026 см-1, ν(NH, амид I) – 1661 см-1, ν(NH, амид II) – 1608 см-1, νas(R–SO2–R) – 1337;1158 см-1, ν(C–N)+∆s(–CH2–) – 1496 см-1, τ(–CH2–) – 1275 см-1 [8].
Валентные колебания группы –OH в диапазоне 3026 см-1 позволяют подтвердить енольную форму лиганда, при этом отсутствуют валентные колебания –C=O. Наблюдаются интенсивные полосы Амид I и Амид II в диапазоне 1661 и 1608 см-1 соответственно. Валентные симметричные (νs) и асимметричные (νas) колебания метиленового звена (–СH2–) присутствуют, но их интенсивность относительно мала. Однако хорошо заметны деформационные симметричные колебания метиленового звена в совокупности с валентными колебаниями связи –C–N в диапазоне 1496 см-1, а также деформационные ножничные колебания –CH2– в диапазоне 1275 см-1. Довольно интенсивные и широкие полосы имеют валентные асимметричные колебания группы –SO2– (тозил). Данная группа разделяется на две полосы с максимумами в диапазоне 1337 см-1 и 1158 см-1.
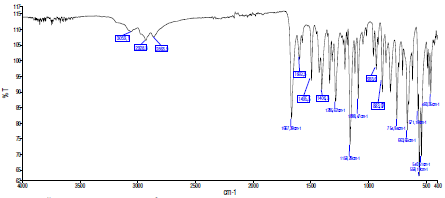
Рис. 6. ИК-спектр бутан-1,4-бис(N-2-тозиламинобензилиден- оксигидразоновой кислоты) (H4L4).
Аналогично в ИК-спектре лиганда H4L4 наблюдается ряд полос поглощения, среди которых следует выделить: ν(OH) – 3059 см-1, ν(NH, Амид I) – 1667 см-1, ν(NH, Амид II) – 1602 см-1, νas(R–SO2–R) – 1336;1159 см-1, ν(C–N)+δs(–CH2–) – 1406 см-1, τ(–CH2–) – 1285 см-1, νas(–CH2–) – 2928 см-1, νs(–CH2–) – 2835 см-1[45].
Валентные колебания группы –OH в диапазоне 3059 см-1 также позволяют подтвердить енольную форму лиганда, при этом также отсутствуют валентные колебания –C=O. Наблюдаются интенсивные полосы Амид I и Амид II в диапазоне 1667 и 1602 см-1 соответственно, которые немного смещены в низкочастотную область. Валентные симметричные (νs) и асимметричные (νas) колебания метиленового звена (–СH2–) присутствуют, по сравнению с лигандом H4L3 их интенсивность больше и составляет 2835 и 2928 см-1 соответственно. Очевидно, что это связано с удлинением полиметиленового спейсера на одну группу –СH2–. Также немного смещены в высокочастотную область и хорошо заметны деформационные симметричные колебания метиленового звена в совокупности с валентными колебаниями связи C–N в диапазоне 1406 см-1. В связи с увеличение длины метиленового спейсера данная полоса также уширяется. Деформационные ножничные колебания –CH2– в диапазоне 1285 см-1, которые практические не смещаются.
При увеличении полиметиленового спейсера валентные асимметричные колебания группы –SO2–(тозил) остаются интенсивными и широкими полосы, а также практически не смещаются. Данная группа снова разделяется на две полосы с максимумами в диапазоне 1336 см-1 и 1159 см-1.
Для подтверждения способа координации были записаны ИК-спектры исследуемых комплексов. ИК-спектры комплексов 1 и 2 представлены на рисунках 7,8.
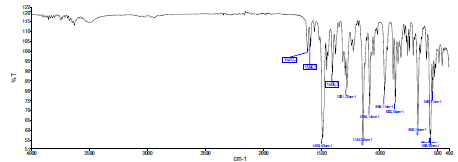
Рис. 7. ИК-спектр комплекса 1.
В ИК-спектре комплекса 1 наблюдается ряд полос поглощения, среди которых следует выделить: ν(NH, Амид I) – 1620 см-1, ν(NH, Амид II) – 1596 см-1, νas(R–SO2–R) – 1281;1142 см-1, ν(C–N)+∆s(–CH2–) – 1490 см-1, τ(–CH2–) – 1281 см-1 [8].
При изучении полученного спектра становится более понятным способ координации лиганда с атомами меди(II). В ИК-спектре данного комплекса исчезает полоса, отвечающая валентным колебаниям гидроксильной группы. Это подтверждает координацию атома меди через депротонизацию енольной формы лиганда. Наблюдаемые интенсивные полосы Амид I и Амид II в ИК-спектре лиганда H4L3 заметно укорачиваются, однако находятся практически в том же диапазоне (1620 и 1596 см-1). Также более смещены в высокочастотную область и имеют большую интенсивность деформационные симметричные колебания метиленового звена ∆s (–CH2–) в совокупности с валентными колебаниями связи –C–N в диапазоне 1490 см-1. Это подтверждает координацию атомов меди(II) через депротонизацию аминного атома азота. Валентные симметричные (νs) и асимметричные (νas) колебания метиленового звена (–СH2–) присутствуют, но, как и в ИК-спектре соответствующего лиганда малоинтенсивны. Деформационные ножничные колебания –CH2– в диапазоне 1281 см-1 практические не смещаются.
Очень интенсивными и широкими полосами также остаются валентные асимметричные колебания группы –SO2–(тозил). Однако одна из полос смещается в высокочастотную область в диапазон 1281 см-1, а другая остается в том же дипазоне практически с той же интенсивностью и составляет 1142 см-1. Смещение одной из полос вероятно вызвано пространственными (стерическими) затруднениями расположения данной группы в пространстве при координировании.
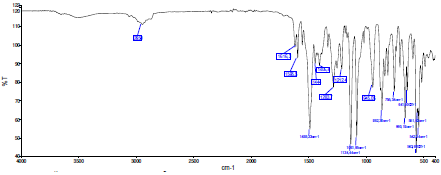
Аналогично в ИК-спектре комплекса 2 наблюдается ряд полос поглощения, среди которых следует выделить: ν(NH, Амид I) – 1616 см-1, ν(NH, Амид II) – 1595 см-1, νas(–CH2–) – 2928 см-1, νas(R–SO2–R) – 1283;1134 см-1, ν(C–N)+∆s(–CH2–) – 1489 см-1, τ(–CH2–) – 1212 см-1 [8].
Рис. 8. ИК-спектр комплекса 2.
В ИК-спектре комплекса 2 также исчезает полоса, отвечающая валентным колебаниям гидроксильной группы, что подтверждает координацию атома меди через депротонизацию енольной формы лиганда. Интенсивность наблюдаемых полос Амид I и Амид II в ИК-спектре лиганда H4L4 заметно уменьшается, однако находятся практически в том же диапазоне (1616 и 1595 см-1). Также более смещены в низкочастотную область и имеют большую интенсивность деформационные симметричные колебания метиленового звена ∆s (–CH2–) в совокупности с валентными колебаниями связи –C–N в диапазоне 1489 см-1. Это в свою очередь также подтверждает координацию атомов меди(II) через депротонизацию аминного атома азота. Ввиду того, что полиметиленовый спейсер увеличился на одну метиленовую группу, валентные асимметричные колебания νas (–СH2–), как и в спектре соответствующего лиганда, также более интенсивны и имеют максимум при 2950 см-1. Валентные симметричные (νs) колебания метиленового звена (–СH2–) малоинтенсивны. Деформационные ножничные колебания –CH2– немного смещены в высокочастотную область и находятся в диапазоне 1212 см-1.
Очень интенсивными и широкими полосами, исследуемого комплекса 2 также остаются валентные асимметричные колебания группы –SO2–(тозил). Однако одна из полос смещается в высокочастотную область в диапазон 1283 см-1, а другая остается в том же дипазоне практически с той же интенсивностью и составляет 1134 см-1. Смещение одной из полос вероятно аналогично вызвано пространственными (стерическими) затруднениями расположения данной группы в пространстве при координации.
Спектр ЭПР жидких растворов исследуемых комплексов в растворе толуол + пиридин представлен на рисунке 9.
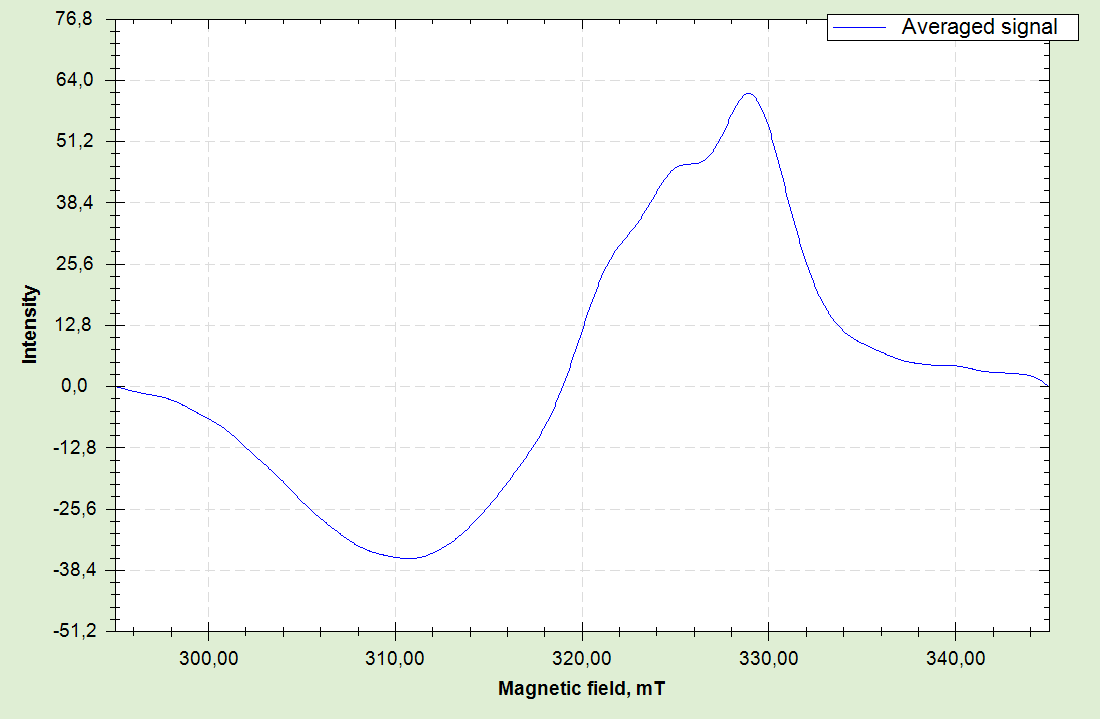
Рис. 9. Спектр ЭПР жидких растворов комплексов 1 и 2.
При комнатной температуре в спектрах ЭПР жидких растворов комплексов 1 и 2 наблюдается широкий плохо разрешенный сигнал сверхтонкой структуры с g-фактором 2,09–2,10 и константой порядка 30 Гс, наблюдаемый для комплексов меди(II) со спейсерированными ацилгидразонами дикарбоновых кислот [9–10]. Величина константы сверхтонкой структуры указывает на реализацию слабых обменных взаимодействий между ядрами катионов меди.
ЗАКЛЮЧЕНИЕ
- Получены исходные лиганды на основе спейсерированных оксигидразоновых кислот – глутаровой и адипиновой. Методом ИК-спеткроскопии подтвержден качественный состав лигандов.
- Синтезированы биядерные комплексы меди(II) со спейсерированными ацилгидразонами кислот. Методами ИК-спектроскопии, термогравиметрического анализа и элементного анализа подтвержден сольватный состав полученных комплексов.
- С помощью спектров ЭПР синтезированных комплексов установлено наличие слабого обменного взаимодействия между атомами меди.
Список литературы
- Калинников В. Т. Современная магнетохимия обменных кластеров / В. Т. Калинников, Ю. В. Ракитин, В. М. Новоторцев // Успехи химии. – 2003. – Т. 72, № 12. – С. 1123–1139.
- Исследование методом ЭПР слабых обменных взаимодействий в биядерных комплексах меди(II) с салицилиденгидразонами / Г. М. Ларин, В. Ф. Шульгин, Е. А. Сарнит [и др.] // Известия РАН. Сер. xим. – 2001. – № 5. – С. 777–783.
- Шульгин В. Ф. Исследование слабых обменных взаимодействий в би-ядерных комплексах меди(II) с ацилдигидразонами 2-гидроксиацетофенона методом ЭПР / В. Ф. Шульгин, А. Н. Гусев, В. Я. Зуб, Г. М. Ларин // Известия РАН. Серия химическая. – 2002. – № 12. – С. 2107–2111.
- Ларин Г. М. Слабые обменные взаимодействия между парамагнитными ионами в мономерных биядерных комплексах ацилдигидразонов / Г. М. Ларин, В. Ф.Шульгин, А. Н. Гусев, В. Я. Зуб // Известия РАН. Серия химическая. – 2003. – № 6. – С. – 1230–1233.
- Шульгин В. Ф. Спектры ЭПР спейсерированных димеров меди(II) на основе ацилдигидразонов 5-бром-2-гидроксиацетофенона и алифатических дикарбоновых кислот / В. Ф. Шульгин, А. Н. Гусев, В. Я. Зуб [и др.] // Известия АН. Сер. xим. – 2005. – № 8. – С. 1752–1757.
- Шульгин В. Ф. Спейсерированные биядерные комплексы меди(II) с ацилдигидразонами алифатических дикарбоновых кислот и 2-гидрокси-5-нитроацетофенона / В. Ф. Шульгин, А. Н. Гусев, А. Н. Чернега [и др.] // Известия АН. Сер. xим. – 2007. – № 2. – С. – 229–233.
- Havanur G. H. Synthesis and characterization of dioxomolibdenum(VI) complexes of dihydrazones / G. H. Havanur, V. B. Mahale // Indian J. Chem. – 1987. – Vol. 26, № 12. – P. 1063–1065.
- ИК спектры основных классов органических соединений [Электронный ресурс]. URL: https://www.chem.msu.su/rus/teaching/tarasevich/Tarasevich_IR_tables_29-02-2012.pdf. (дата обращения: 15.03.2025).
- Ракитин Ю. В. Интерпретация спектров ЭПР координационных соединений / Ю. В. Ракитин, Г. М. Ларин, В. В. Минин. – М.: Наука, 1993. – 399 с.
- Яблоков Ю. В. Парамагнитный резонанс обменных кластеров / Ю. В. Яблоков, В. К. Воронкова, Л. В. Мосина – М.: Химия, 1988. –181 с.
BINUCLEAR COPPER(II) COMPLEXES BASED ON SPACERED OXYHYDRAZONIC ACIDS
Goncharuk D. E., Shulgin V. F., Gusev A. N.
Institute of biochemical technologies, ecology and pharmacy (structural division) of the Federal State
Autonomous Educational Institution of Higher Education «V. I. Vernadsky Crimean Federal
University», Simferopol, Russia
E-mail: goncharykd0@gmail.com
The most interesting group of polynuclear complexes consists of binuclear compounds exhibiting unusual magnetic properties that are not limited to the magnetism characteristic of mononuclear compounds or diamagnetism typical of clusters with strong metal-metal bonds. The reason for these magnetic properties is the so-called exchange interactions, which are quantum effects that cause the correlated behavior of the spins of unpaired electrons. The nature of spin-spin interactions in dimers and exchange clusters depends on the details of the geometric and electronic structure of compounds and has a decisive effect on their magnetic properties.
When studying weak interactions, the use of EPR spectroscopy methods is quite productive. This method is particularly useful in the study of copper(II) dimeric complexes. Coordination compounds, which have exchange interactions between metal ions separated by a distance of more than 3 Ǻ, characteristic of most exchange dimers, have recently attracted increased interest. A large number of exchangeable dimers have been described in the literature, whereas data on complexes with a distance between paramagnetic ions of more than 3 Ǻ are limited. The latter are particularly interesting in the study of exchange interactions, since they allow quite smoothly changing the distance between paramagnetic centers and modifying the geometry and electronic nature of the coordination polyhedron, as well as the bridge group (aliphatic, unsaturated, or aromatic spacers). In this paper, spacered oxyhydrazonic acids are considered as potential ligands, in which it is possible to note some structural features and the ability to smoothly change the distance between copper(II) cations, as well as the obtained binuclear copper(II) complexes based on spaced acylhydrazones of some dicarboxylic acids.
Binuclear complexes of copper(II) with spacered acylhydrazones of acids were obtained. The solvate composition of the complexes [Cu2L3(py)2]∙6H2O and [Cu2L4(py)2]∙6H2O was confirmed by thermogravimetric and elemental analysis. To study the method of ligand coordination, the IR spectra of the obtained complexes were recorded. In the EPR spectra of the synthesized complexes, a weakly resolved CTC with a constant of the order of 30 Hz is observed, which is characteristic of copper(II) dimers with a weak exchange interaction between metal nuclei.
Keywords: copper(II) binuclear complexes, IR spectra, electron paramagnetic resonance, ultrathin structure, exchange interaction.
References
- Kalinnikov V. T., Rakitin Yu. V., Novotortsev V. M., Modern magnetochemistry of exchange clusters, Successes of Chemistry, 72 (12), 1123 (2003). (in Russ.).
- Larin G. M., Shulgin V. F., Sarnit E. A., EPR study of weak exchange interactions in binuclear copper(II) complexes with salicylidene hydrazones, News of the Russian Academy of Sciences. The chemical series, 5, 777 (2001). (in Russ.).
- Shulgin V. F., Gusev A. N., Zubov V. Ya., Larin G. M., Investigation of weak exchange interactions in bi-nuclear complexes of copper(II) with acyldihydrazones of 2-hydroxyacetophenone by EPR method, News of the Russian Academy of Sciences. The chemical series, 12, 2107(2002). (in Russ.).
- Larin G. M., Shulgin V. F., Gusev A. N., Zubov V. Ya., Weak exchange interactions between paramagnetic ions in monomeric binuclear complexes of acyl dihydrazones, News of the Russian Academy of Sciences. The chemical series, 6, 1230 (2003). (in Russ.).
- Shulgin V. F., Gusev A. N., Zubov V. Ya. [et al.], EPR spectra of spacered copper(II) dimers based on 5-bromo-2-hydroxyacetophenone acyl dihydrazones and aliphatic dicarboxylic acids, News AN. Ser. chem., 8, 1752 (2005). (in Russ.).
- Shulgin V. F., Gusev A. N., Chernega A. N., [et al.], Spacered binuclear complexes of copper(II) with acyl dihydrazones of aliphatic dicarboxylic acids and 2-hydroxy-5-nitroacetophenone, News AN. S. chem., 2, 229 (2007). (in Russ.).
- Havanur G. H., Mahale V. B., Synthesis and characterization of dioxomolibdenum(VI) complexes of dihydrazones, Indian J. Chem., 26 (12), 1063 (1987).
- IR spectra of the main classes of organic compounds, https://www.chem.msu.su/rus/teaching/tarasevich/Tarasevich_IR_tables_29-02-2012.pdf (Accessed March 15, 2025). (in Russ.).
- Rakitin Yu. V., Larin G. M., Minin V. V., Interpretation of EPR spectra of coordination compounds, (Science, Moscow, 1993). (in Russ.).
- Yablokov Yu. V., Voronkova V. K., Mosina L. V., Paramagnetic resonance of exchange clusters, (Chemistry, Moscow, 1972). (in Russ.).