ХИМИЧЕСКИЕ НАУКИ
Ученые записки Крымского федерального университета имени В. И. Вернадского
Биология. Химия. Том 11 (77). 2025. № 1. С. 273–282.
УДК 546.47+ 542.97
DOI 10.29039/2413-1725-2025-11-1-273-282
МОНОЯДЕРНЫЙ КОМПЛЕКС ЦИНКА C ТЕТРАДЕНТАТНЫМ N2O2-ДОНОРНЫМ ЛИГАНДОМ КАК ПЕРСПЕКТИВНЫЙ МАТЕРИАЛ ДЛЯ БИОВИЗУАЛИЗАЦИИ
Брага Е. В., Мамонтов К. М., Сидякин А. И., Гусев А. Н.
Институт биохимических технологий, экологии и фармации (структурное подразделение)
ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского», Симферополь,
Республика Крым, Россия
E-mail: braga.yelena@ya.ru
Синтезирован и исследован люминесцирующий комплекс цинка на основе азометинового «salen-like» лиганда, который представляет собой две молекулы 3-метил-1-фенил-4-формилпиразол-5-она «сшитые» молекулой пропан-1,3-диамина. Состав и структура комплекса установлена по данным элементного, термогравиметрического анализа, ИК-спектроскопии. Молекулярная структура комплекса установлена на основе данных РСА. Комплекс проявляет интенсивную фотолюминесценцию в растворах и может использоваться для визуализации клеточных структур клеток эпидермиса Allium cepa.
Ключевые слова: люминесценция, цинк, биовизуализация.
ВВЕДЕНИЕ
Современное развитие медицины, молекулярной биологии и генетики тесно связано с совершенствованием методов визуализации молекулярных процессов, протекающих в клетках живых организмов. В данном направлении особенно перспективным является метод флуоресцентной микроскопии, обеспечивающий высокое пространственное разрешение и хорошую чувствительность. Учитывая приборные возможности и специфику объектов исследования многие коммерческие флуорофоры на основе органических красителей не отвечают высоким требованиям современной диагностики, среди которых наиболее важными являются: обеспечение специфической связи с молекулой-мишенью, органеллой или клеткой; высокая эффективность излучения в сочетании с фотостабильностью. Кроме вышеуказанных требований в последнее десятилетие возрос спрос к люминофорам, чувствительным к конкретным мишеням: биометаллам, рН среды, биомаркерам [1].
Высокая люминесцентная активность азометиновых оснований в присутствии ионов цинка, в сочетании с устойчивостью в растворах, чувствительностью к рН среды и наблюдаемой двухфотонной люминесценцией, делает предложенные соединений идеальными кандидатами для использования в биоимейджинге. Цинк относится к группе микроэлементов, его уникальность заключается в том, что он входит в состав более 300 ферментов и выполняет разнообразные физиологические функции, обладает антиоксидантными свойствами. Его токсичность для животных и человека невелика – это связано с тем, что при избыточном поступлении он выводится организмом. Таким образом, люминесцирующие в видимой области комплексы цинка являются перспективными красителями для биовизуализации [2]. Ранее были описаны комплексы цинка с азометиновыми производными салицилового альдегида, демонстрирующие высокую эффективность для визуализации живых клеток. Очевидно, что варьирование заместителей в подобных соединениях является удобным способом настройки как фотофизических характеристик, так и улучшения параметров бивизуализации. В настоящей работе описан комплекс цинка с азометиновым производным 1-фенил-3-метилпиразол-5-она и 1,3-диаминопропана, люминесцентные свойства которого позволяют его использовать в флуоресцентной микроскопии высокого разрешения [3].
МАТЕРИАЛЫ И МЕТОДЫ
В работе использованы: 1-фенил-3-метилпиразол-5-он, пропан-1,3-диамин фирм (Merck), Zn(CH3COO)2∙2H2O (ч.д.а.), гидроксид натрия (х.ч.), гидроксид калия (х.ч.), соляную кислоту (х.ч.), хлорангидрид ортофосфорной кислоты (х.ч.), этилацетат(х.ч.).
Элементный анализ синтезированных соединений выполнен на CHN-анализаторе «Euro EA Elemental Analisyer». Термогравиметрические исследования синтезированных комплексов выполнены на термогравиметрическом дифференциальном термическом анализаторе «STA 6000». Инфракрасные спектры зарегистрированы на ИК-Фурье спектрометре «Perkin Elmer Spectrum-two». Спектры возбуждения и люминесценции зарегистрированы на спектрофлуориметре «Horiba Fluoromax-4». Определение структуры монокристаллов методом рентгеновской дифракции проводили на приборе «Bruker Apex-II CCD» с дифрактометром Xcalibur, Eos (МоКα-излучение, графитовый монохроматор, λ = 0,71073 Ǻ). Структура была определена прямым методом и уточнены полноматричным методом наименьших квадратов в анизотропном приближении (SHELX-97 и SHELX-2014) [4]. 1Н-ЯМР-спектры (δ, м.д.; КССВ, Гц) получены для растворов в DMSO-d6 на приборе «Varian Mercury-400» (400 МГц), внутренний стандарт – Me4Si. ESI+-MS сняты на Thermo Scientific MS/MS TSQ Quantum Access MAX.
Клетки исследовали на люминесцентном микроскопе «МИКМЕД-2вар.26» (ЛОМО-Микросистемы, Россия). Фотофиксацию вели с использованием цифровой камеры «MC-6.3» (ЛОМО-Микросистемы, Россия) интегрированную с программным обеспечением «ToupView» (ToupTek Photonics).
Синтез координационного соединения. К раствору 4-формил-3-метил-1-фенилпиразол-5-она (808 мг, 4 ммоль) в 50 мл метанола добавляли 2 ммоль соответствующего диамина и перемешивали при кипячении с обратным холодильником в течение 1 часа. После этого к раствору добавляли кристаллический Zn(AcO)2·2H2O (438 мг, 2 ммоль) и раствор Et3N (400 мг, 4 ммоль) в 10 мл метанола. Перемешивали при 50 °C в течение 8 часов. Осадок отфильтровали, промыли холодным метанолом и эфиром и сушили на воздухе. После перекристаллизации из этанола выход продукта составил 67 %.
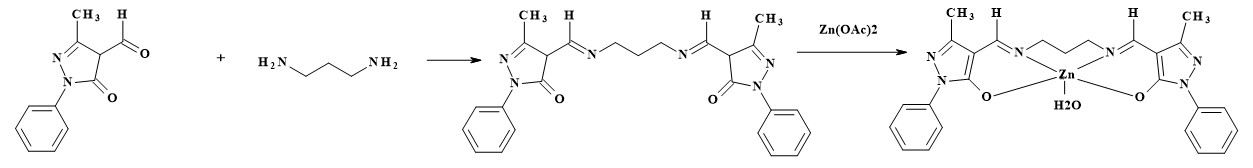
Рис.1. Схема синтеза координационного соединения.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Целевой комплекс был получен с хорошим выходом в одну стадию в виде бесцветного кристаллического соединения, умеренно растворимого в этаноле, хлороформе, ацетонитриле, хорошо растворимое в ДМСО и нерастворимого в воде.
Состав синтезированного комплекса определяли методами элементного и термогравиметрического анализа. По данным элементного анализа комплекс имеет состав ZnLꞏH2O. Для C25H26N6O3Zn вычислено в %: C, 57.31; H, 5.00 %; N, 16.04. Найдено: C, 57.40; H, 5.15, N, 16.07. По данным ТГА установлено, что в интервале температур 180–200 °С, происходит потеря массы на 4 %, сопровождающаяся эндотермическим эффектом. Это соответствует удалению координированной молекулы воды. Соединение термически стабильно до температуры 400 °С. Нагревание выше 400 °C приводит к медленному разложению образца.
ИК-спектр комплекса (рис. 2) позволяет оценить таутомерную форму лиганда и способ координации с атомом металла. В спектре наблюдаются полосы колебаний в области 2847–2922 и 3028–3059 см-1, отнесенные к связям C–H алифатической цепи и ароматических колец, соответственно. Интенсивная полоса при 1628 см-1 указывает на наличие группы C=N, принадлежащей к иминной группе, в то время как полоса при 1363 см-1 отвечает валентным колебаниям Cpyr–O. Регистрация данных полос указывает на образование депротонированной иминольной формы лиганда при координации с катионом цинка [5, 6]. Примечательно, что ИК-спектр демонстрирует широкий пик в интервале 3200–3300 см-1, указывающий на наличие координированной молекулы воды в структуре комплекса. Кроме того, полосы, наблюдаемые в низкочастотных областях 510 и 455 см-1 отвечают колебаниям ν (Zn–N) и ν (Zn–О) соответственно, что подтверждает образование координационных связей.
Рис. 2. ИК-спектр комплекса.
1H ЯМР-спектр диамагнитного комплекса цинка(II) (рис. 3) дает дополнительное подтверждение того, что азометиновый лиганд координируется в депротонированной иминольой форме. Альдегидный протон (–CH=О) проявился в виде синглета при 8,19 ppm, при этом в спектре отсутствуют сигналы «кислых» протонов. Пики, наблюдаемые в спектре 1Н ЯМР, согласуются с общим числом атомов водорода, присутствующих в структуре. Эти данные свидетельствуют о том, что комплекс остается стабильным в растворе и не подвергается диссоциации.
Рис. 3. 1H ЯМР-спектр комплекса цинка(II).
Молекулярное строение комплекса установлено по данным РСА.
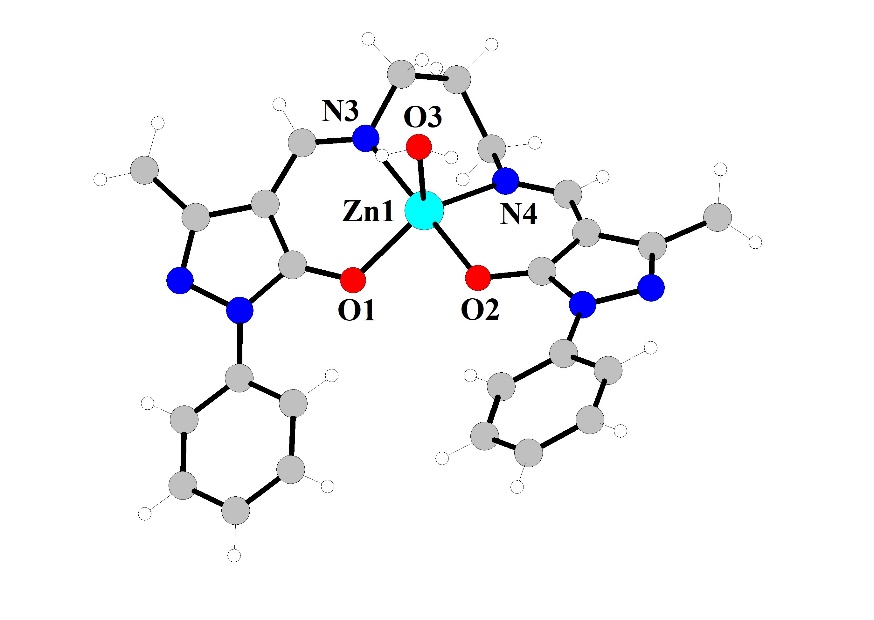
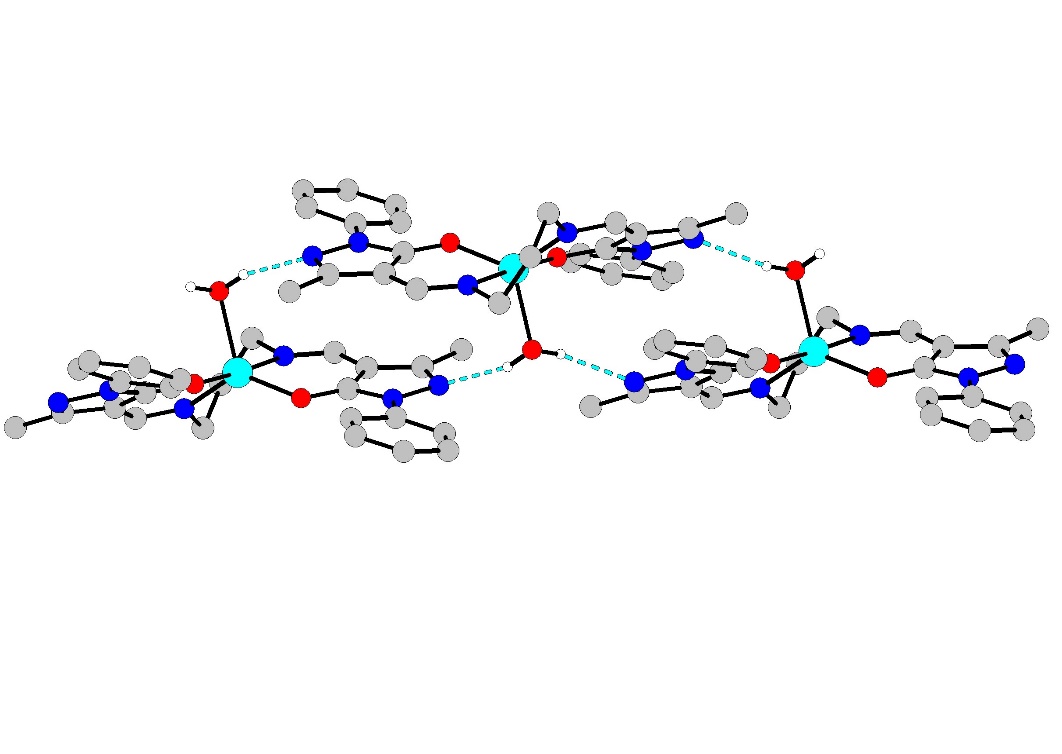
Рис. 4. Молекулярное строение и фрагмент кристаллической решетки комплекса.
Комплекс является молекулярным и кристаллизуется в триклинной сингонии. Параметры решетки: a=7.2840(2), b=11,4657(3), c=14.5993(4), α=74.4730(10), β=75.8820(10), γ=82.8380(5), V3=1136.99(5), Z=2. Катион цинка в комплексе пентакоординирован за счет двух атомов азота и двух атомов кислорода полностью депротонированной тетрадентатной молекулы лиганда. Пятое место в координационной сфере занимает атом кислорода молекулы воды. Координационный полиэдр представляет собой искаженную тетрагональную пирамиду. Длины связей близки к стандартным значениям. Отдельные молекулы комплекса соединены водородной связью c участием атомов водорода координированной молекулы воды одной молекулы комплекса и атомов азота пиразольных колец соседних молекул (O3H3A–N2 (d=1,926 Å) и O3H3B–N5 (d=2,047 Å), что приводит к образованию 1D-супрамолекулярной структуры.
Основным показателем, характеризующим эффективность флуоресцентного красителя, является эффективная фотолюминесценция при возбуждении в ближней УФ- или видимой областях спектра [7]. Флуоресцентные свойства были исследованы для растворов комплекса в хлороформе и ДМСО (5·10-5 М). На первом этапе были исследованы спектры поглощения в указанных растворах (рис. 5). В обоих случаях в спектрах наблюдаются две основные полосы поглощения с максимумами 276 и 285 нм и 309 и 347 нм для растворов в хлороформе и ДМСО соответственно. Согласно литературным данным коротковолновая полоса может быть отнесена к π–π* переходам ароматических колец, в то время как длинноволновая полоса относится к n–π* переходам связи C=N. Отличительной чертой спектров является достаточной большой длинноволновый «хвост» в спектре, заходящий в видимую область, очевидно связанный с появлением MLCT полосы и указывающий на возможность поглощения комплексов относительно безопасных для живых клеток квантов видимого спектра [7].

Рис. 5. Спектры поглощения растворов комплекса в хлроформе (пунктирная крисвая) и ДМСО (сплошная кривая).
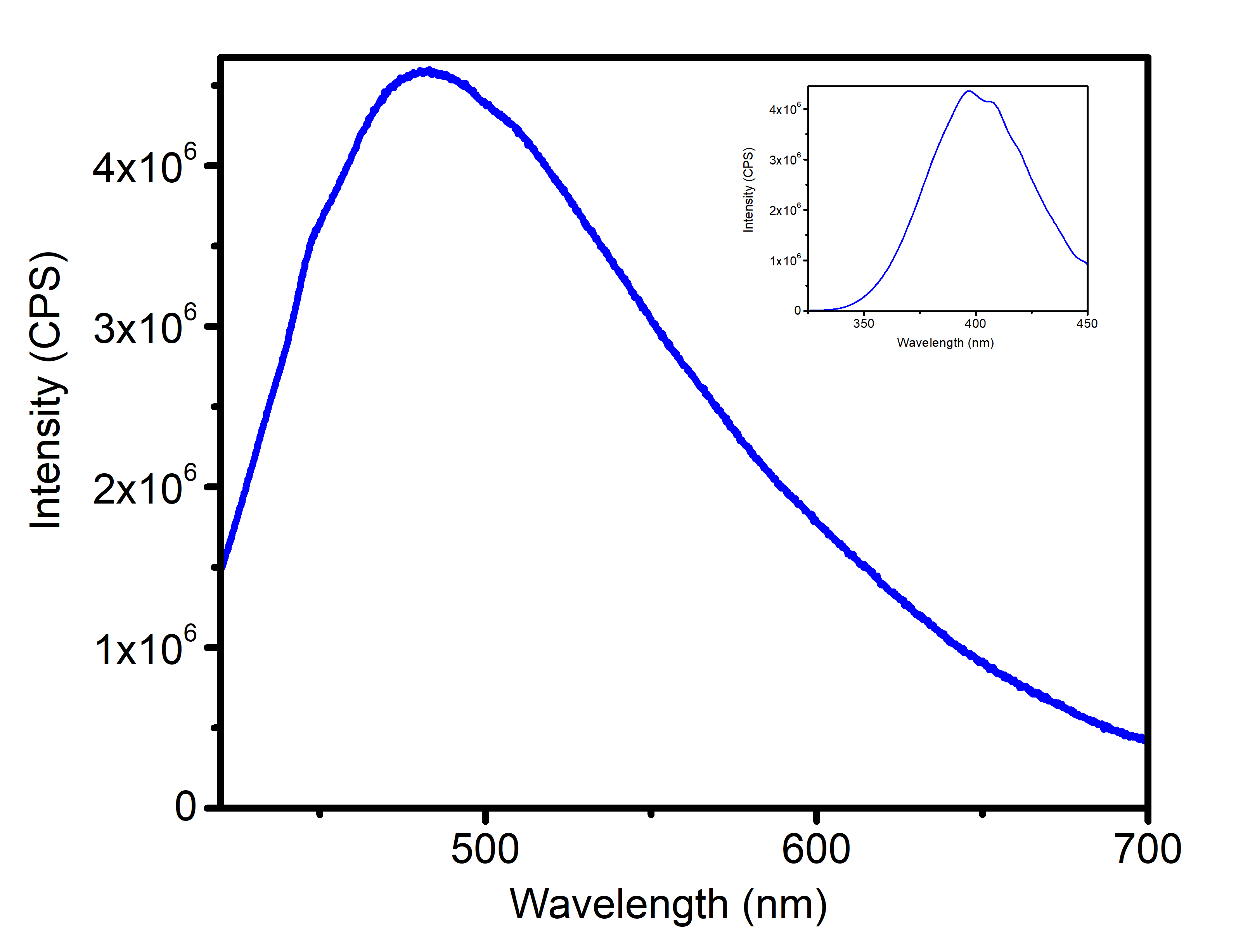
Оптимальная длина возбуждения для растворов комплексов была установлена по данным спектроскопии возбуждения, согласно которой в хлороформе максимум эмиссии достигается при возбуждении 354 нм, в то время как для раствора в ДМСО максимумы в спектре возбуждения расположены при 397 и 407 нм. При облучении светом с соответствующей длинной волны комплексы проявляют яркую эмиссию в синей и сине-зеленой областях спектра. Спектры люминесценции представлены на рисунке 6, из которого видно, что в обоих случаях спектр представляет собой интенсивную широкую полосу с двумя максимумами (444 и 452 нм) для хлороформного раствора и одним максимумом при 482 нм для раствора в ДМСО. Квантовый выход излучения составляет 0,7 и 0,9 % для раствора в хлороформе и ДМСО, соответственно.
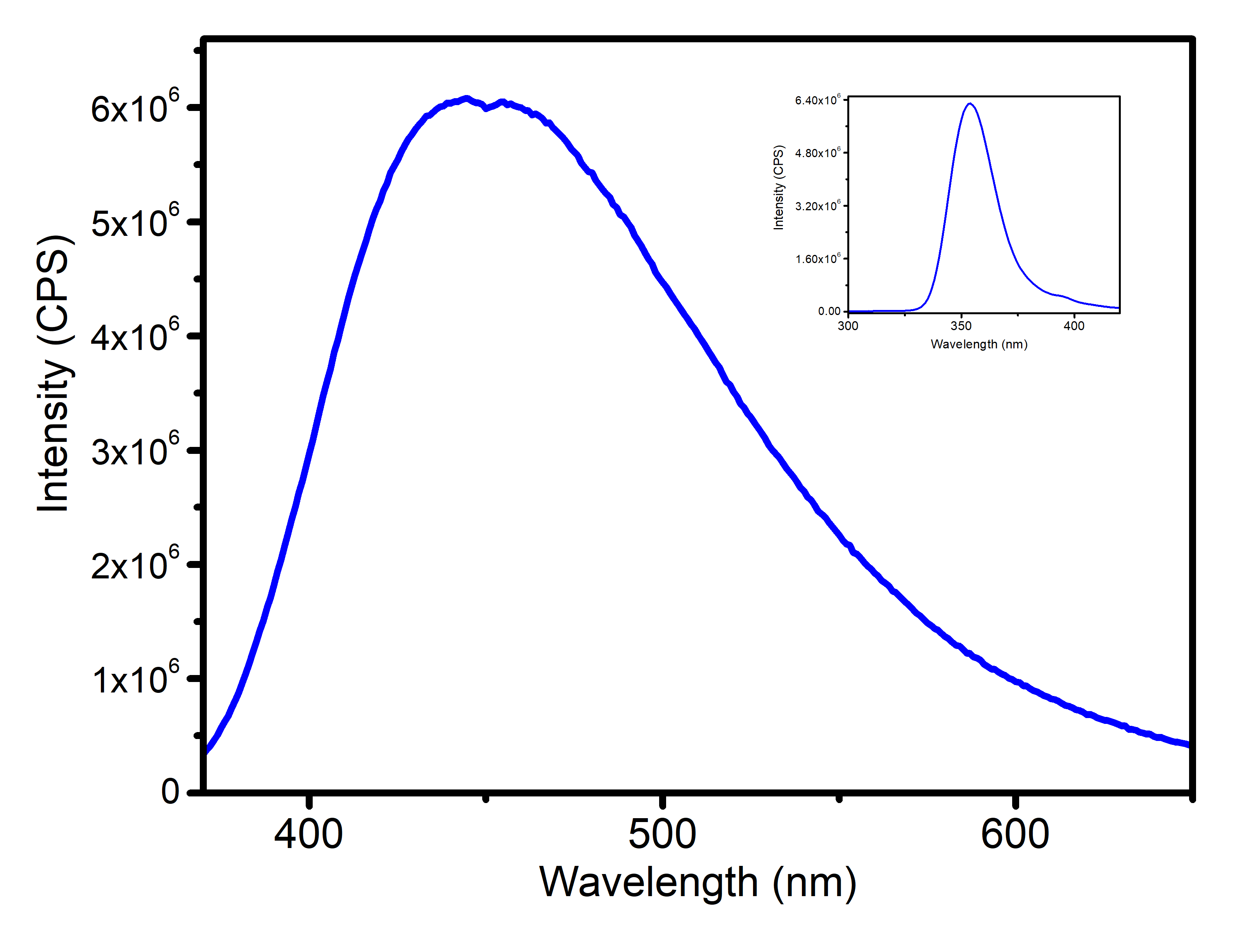 |  |
| а | б |
| Рис. 6. Спектры люминесценции и возбуждения (вставка) для растворов комплекса в хлороформе (а) и ДМСО (б). | |
Время жизни возбужденного состояния находится наносекундном диапазоне, что указывает на флуоресцентный характер излучения. Кривые затухания аппроксимируются биэкспоненциальными выражениями.
Таблица 1
Фотофизические характеристики растворов комплекса
| Растворитель | Поглощение, нм | Максимум эмиссии, нм | Квантовый выход, % | Время жизни, нс |
| Хлороформ | 276, 309 | 444, 452 | 0,7 | 5,4 |
| ДМСО | 285, 347 | 482 | 0,9 | 6,5 |
Учитывая, что исследованный комплекс проявляет более эффективную фотолюминесценцию в ДМСО при возбуждении видимым светом испытания по биовизуализации проводили в данном растворителе [8]. Комплекс растворяли в 80 % ДМСО (1 г/л), и в соотношении 1:10 вносили в химически чистый глицерин. Клетки эпидермиса лука (Allium cepa L.) отделяли от луковиц и сразу переносили в глицериновый раствор красителя. Спустя 24 часа после достаточной диффузии красителя в клетки исследовали их на люминисцентном микроскопе. В клетках чётко визуализируются клеточная оболочка, ядра и ядрышки, цитоплазма (в пристенных слоях клетки) (рис. 7.). Взаимодействие носит адсорбционный характер.
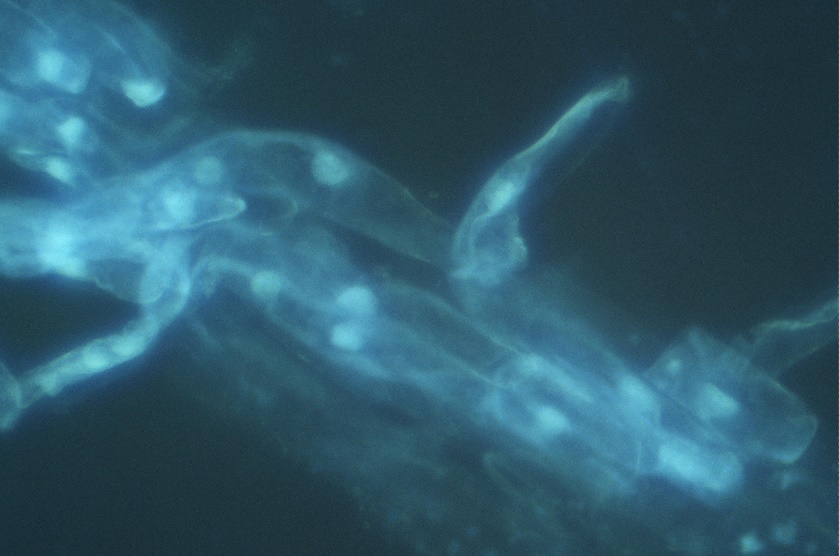 |
| Рис. 7. Флуоресценция после окрашивания (увеличение ×400). Условия визуализации: спектр возбуждающего света: 400–410 нм; барьерный светофильтр (дихроическое зеркало) 400–455нм; снимаемый спектр флуоресценции 455–700 нм. |
ЗАКЛЮЧЕНИЕ
- Синтезирован комплекс цинка на основе 3-метил-1-фенил-4-формилпиразол-5-она и пропан-1,3-диамина. Состав комплекса установлен по данным элементного и термогравиметрического анализа, ЯМР-спектроскопии. Строение комплекса установлено методами ИК-спектроскопии и РСА.
- Установлено, что комплекс проявляет интенсивную фотолюминесценцию в синей области спектра.
- Полученное соединение является эффективным красителем для визуализации биологических объектов.
“Работа выполнена при поддержке гранта РНФ №25-23-00143”
Список литературы
- Lo K.K.-W. Applications of luminescent inorganic and organometallic transition metal complexes as biomolecular and cellular probes / K.K.-W. Lo, A.W.-T. Choi, W.H.-T. Law // Dalt. Trans. The Royal Society of Chemistry – 2012. – Vol. 41, № 20 – P. 6021–6047.
- LITE microscopy: Tilted light-sheet excitation of model organisms offers high resolution and low photobleaching / T. C. Fadero, T. M. Gerbich, K. Rana [et al] // The Journal of Cell Biology. – 2018. –Vol. 217. – P. 1869–1882.
- Dumur F. Low-cost zinc complexes for white organic light-emitting devices / F. Dumur, L. Beouch,
M.-A. Tehfe, [et al.] // Thin Solid. Films. – 2014 – Vol. 564.– P. 351–360. - Sheldrick G. M. SHELX97. Program for the Solution of Crystal Structures. Göttingen University, Göttingen (Germany), 1997.
- Marchetti F., Pettinari C., Di Nicola C., Tombesi A., Pettinari R. Coordination chemistry of pyrazolone-based ligands and applications of their metal complexes. Coord. Chem. Rev. – 2009. – Vol. 401. – 213069.
- Orabi E. A. Tautomerism and antioxidant activity of some 4-acylpyrazolone-based Schiff bases: a theoretical study / E. A. Orabi // RSC Advances. – 2018. – Vol. 8, № 54. – P. 30842–30850.
- Kumar N. Roopa, Vandana Bhalla V., Kumar M. Beyond zinc coordination: Bioimaging applications of Zn(II)-complexes, Coord. Chem.Rev. – 2021. – Vol. 427. – P. 2133550.
- Chan J., Dodani S. C., Chang C. J. Reaction-based small-molecule fluorescent probes for chemoselective bioimaging. Nat. Chem. – 2012. – Vol. 4. – P. 973–984.
MONONUCLIAR COMPLEX OF ZINK WITH TETRADENTATE N2O2-DONOR LIGAND AS A PERSPECTIVE MATERIAL FOR BIOIMAGING
Braga E. V., Mamontov K. M., Sidyakin A. I., Gusev A. N.
V. I. Vernadsky Crimean Federal University, Simferopol, Crimea, Russian Federation
E-mail: braga.yelena@ya.ru
Modern development of medicine, molecular biology and genetics is closely related to the improvement of methods for visualization of molecular processes occurring in the cells of living organisms. The fluorescence microscopy method, which provides high spatial resolution and good sensitivity, is particularly promising in this direction. Taking into account the instrumental capabilities and specificity of research objects, many commercial fluorophores based on organic dyes do not meet the high requirements of modern diagnostics, among which the most important are: ensuring specific binding to the target molecule, organelle or cell; high emission efficiency combined with photostability. In addition to the above-mentioned requirements, in the last decade the demand for phosphors sensitive to specific targets: biometals, pH of the medium, biomarkers has increased. The high luminescent activity of azomethine bases in the presence of zinc ions, combined with stability in solutions, sensitivity to the pH of the medium and observed two-photon luminescence, makes the proposed compounds ideal candidates for use in bioimaging. Zinc belongs to the group of trace elements, its uniqueness lies in the fact that it is a part of more than 300 enzymes and performs a variety of physiological functions, has antioxidant properties. Its toxicity for animals and humans is small – this is due to the fact that in excessive intake it is excreted by the body. Thus, zinc complexes luminescent in the visible region are promising dyes for biovisualization.
A luminescent zinc complex based on azomethine “salen-like” ligand, which represents two molecules of 3-methyl-1-phenyl-4-formylpyrazol-5-one “cross-linked” by a molecule of propane-1,3-diamine, has been synthesized and studied. The composition and structure of the complex was established by elemental, thermogravitetric analysis and IR spectroscopy. The molecular structure of the complex was established on the basis of PCA data. The complex exhibits intense photoluminescence in solutions and can be used for visualization of cellular structures of A. cepa epidermis cells.
Keywords: luminescence, zinc, bioimaging.
References
- Lo, K. K.-W., Choi, A. W.-T., & Law, W. H.-T., Applications of luminescent inorganic and organometallic transition metal complexes as biomolecular and cellular probes. Dalton Transactions, 41(20), 6021 (2012).
- Fadero T. C., Gerbich T. M., Rana K., Suzuki A., DiSalvo M., Schaefer K. N., Maddox P. S. LITE microscopy: Tilted light-sheet excitation of model organisms offers high resolution and low photobleaching. The Journal of Cell Biology, 217(5), 1869 (2018).
- Dumur F., Beouch L., Tehfe M.-A., Contal E., Lepeltier M., Wantz G., Gigmes D. Low-cost zinc complexes for white organic light-emitting devices. Thin Solid Films, 564, 351 (2014).
- Sheldrick G. M. SHELX97. Program for the Solution of Crystal Structures. Göttingen University, Göttingen (Germany), (1997).
- Marchetti F., Pettinari C., Di Nicola C., Tombesi A., Pettinari R. Coordination chemistry of pyrazolone-based ligands and applications of their metal complexes. Coord. Chem. Rev. 401, 213069 (2011).
- Orabi E. A. Tautomerism and antioxidant activity of some 4-acylpyrazolone-based Schiff bases: a theoretical study. RSC Advances. 8 (54), 30842 (2018).
- Kumar N, Roopa, Vandana Bhalla V., Kumar M. Beyond zinc coordination: Bioimaging applications of Zn(II)-complexes, Coord. Chem.Rev., 427, 213550 (2021).
- Chan J., Dodani S. C., & Chang C. J. Reaction-based small-molecule fluorescent probes for chemoselective bioimaging. Nature Chemistry, 4(12), 973 (2012).



