ANTIBACTERIAL ACTIVITY OF 3-ARILYMINOMETHYLCHROMONES
JOURNAL: «SCIENTIFIC NOTES OF V.I. VERNADSKY CRIMEAN FEDERAL UNIVERSITY. Biology. Chemistry» Volume 6 (72), №3, 2020
Publication text (PDF):Download
UDK: 547.814.1:615.28
AUTHOR AND PUBLICATION INFORMATION
AUTHORS:
Khaeva O. E., FSBEI HE North Ossetian State University named after Kosta Levanovich Khetagurov, Vladikavkaz, Russia
Ikoeva L. P., Federal Agency of Scientific Organizations North Caucasus Research Institute of Mountain and Foothill Agriculture, RAS, village Mikhaylovskoye, Russia
TYPE:Article
DOI:https://doi.org/10.37279/2413-1725-2020-6-3-256-261
PAGES:from 256 to 261
STATUS:Published
LANGUAGE:Russian
KEYWORDS: 3–aryliminomethylchromone, antibacterial activity, antibiotics, Staphulococcus aureus strain, Bacillus subtilis strain, Escherichia coli strain, Pseudomonas aeruginosa strain.
ABSTRACT (ENGLISH):
In conditions of multiple drug resistance of microorganisms to recently used drugs, the search for new chemotherapeutic agents with a pronounced bactericidal or bacteriostatic effect with low toxicity and teratogenicity remains relevant. Chromone derivatives with a wide spectrum of pharmacological activity (membrane-stabilizing, antiviral, antibacterial, anti-inflammatory, cardioprotective, antioxidant) are promising compounds for the search for new generation chemotherapeutic drugs.
As a result of the study, it was found that gram-positive bacteria Staphylococcus aureus shows the highest sensitivity to the studied compounds when growing on a liquid nutrient medium. The studied compounds are also active against pathogenic strains of Bacillus cereus, Escherichia coli. The minimum inhibitory concentration (IPC) of the most active substances in relation to St. strains aureus is 10 μg/ml for 7-acetoxy-3-(p-bromophenyl)iminomethylchromone, and for 3-(p-bromophenyl)-iminomethylchromone and 7-acetoxy-3-(p-sulfamidophenyl)iminomethylchromone – 20 μg/ml. For 7-acetoxy-3- (p-bromophenyl)iminomethylchromone and 3-(p-bromophenyl)iminomethylchromone, a high antibacterial activity was revealed with respect to the spore-forming bacteria Bacillus subtilis – MPC – 20 μg / ml. The synthesized compounds exhibit a low bacteriostatic activity with respect to the Pseudomonas aeruginosa strain.
Experimental studies have shown that the nature and position of substituents in the structure of 3–aryliminomethylchromones affects their antibacterial activity against strains of gram-positive bacteria Staphulococcus aureus and Bacillus subtilis, a strain of gram-negative bacteria: Escherichia coli. The presence in the series of synthesized 3–aryliminomethylchromones of compounds with high bacteriostatic activity at the level of an antibacterial drug from the group of sulfonamides – norsulfazole was established.
ВВЕДЕНИЕ
В настоящее время основным методом борьбы с патогенными и условно-патогенными бактериями – возбудителями инфекционных заболеваний является использование различных групп химиотерапевтических препаратов с выраженной антибактериальной активностью, наиболее эффективными из которых по-прежнему остаются природные антибиотики и их синтетические аналоги. К сожалению, повсеместно применяемая антибиотикотерапия имеет ряд негативных последствий, одно из которых проявляется в формировании множественной лекарственной устойчивости микроорганизмов к еще недавно успешно применяемым лекарственным препаратам [1]. В связи с этим поиск новых химиотерапевтических средств, обладающих выраженным бактерицидным или бактериостатическим эффектом, по-прежнему сохраняет свою актуальность. При разработке и получении химиотерапевтических препаратов новых поколений перспективным является химическая модификация различных органических соединений с защищенными от воздействия бактериальных энзимов активными радикалами, что позволяет расширить спектр их действия для решения проблемы резистентности.
Цель данной работы – изучение уровня антибактериальной активности
3–арилиминометилхромонов в отношении штаммов Staphуlococcus aureus, Bacillus subtilis, Escherichia coli, Pseudomonas aeruginosa как наиболее характерных представителей грамположительных и грамотрицательных бактерий.
МАТЕРИАЛЫ И МЕТОДЫ
В ходе исследования был испытан ряд новых синтетических веществ с предполагаемыми антибактериальными свойствами – 3–арилиминометилхромонов (рис. 1), полученных по методике, представленной в работе [2]. Производные хромона, обладающие высоким спектром фармакологической активности, находят широкое применение в медицинской практике в качестве мембраностабилизирующих, антибактериальных, противовоспалительных, кардиопротекторных, антиоксидантных средств [2–4].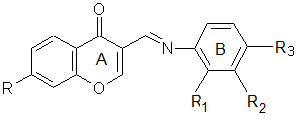
Рис. 1. Общая структурная формула 3–арилиминометилхромонов, где
G1: R= R1= R2=H, R3=Br; G 2: R= R1= R2=H, R3=SO2NH2;
G 3: R= R2= R3=H, R1=COOH; G4: R= R1=H, R2= OH, R3=COOH;
G5: R= R1=R3=H, R2=NO2; G6: R= OAc, R1= R2=H, R3=COOH;
G7: R= OAc, R1=COOH, R2= R3=H; G8: R= OAc, R1= R2=H, R3=Br;
G9: R= OAc, R1= R2=H, R3=SO2NH2; G10: R= OAc, R1= R3=H, R2=NO2.
Структура синтезированных соединений установлена на основании данных элементного анализа, ИК и ПМР спектроскопии.
В качестве тест-объектов при исследовании антимикробной активности
3–арилиминометилхромонов использовали штаммы представителей грамположительных бактерий: Staphуlococcus aureus 209p, Staphуlococcus aureus (Макаров), Bacillus subtilis L – 2; грамотрицательных бактерий: Escherichia coli F–50, Pseudomonas aeruginosa 9027. Бактериостатическое действие исследуемых веществ исследовали по общепринятой в микробиологии методике – методом серийных разведений в жидкой питательной среде – мясо-пептоном бульоне [4, 5] нагрузке 300000 микробных тел в 1 мл. Результаты эксперимента учитывали после инкубации при температуре 37 ºС через 24 ч. Наименьшую концентрацию соединения, задерживающую рост микроорганизмов, принимали за минимальную подавляющую концентрацию (МПК)
В качестве эталона сравнения использовали применяемый в медицинской практике антибактериальный препарат из группы сульфаниламидов – норсульфазол.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Результаты исследования антибактериальной активности 3–арилиминометилхромонов представлены в таблице 1.
В результате проведённого исследования было выявлено, что наиболее высокую чувствительность к исследуемым соединениям проявляют грамположительные бактерии: St. aureus при росте на жидкой питательной среде. При инкубации штаммов Staphуlococcus aureus на мясо-пептоном бульоне с 7–ацетокси–3–(п–бромфенил)–иминометилхромоном (соединение G8) визуально отмечалась наибольшая прозрачность бактериальной взвеси по сравнению с контролем. Минимальные подавляющее концентрации наиболее активных веществ в отношении к штаммам St. aureus составляет для соединения (G8) – 10 мкг/мл и для соединений (G1, G9) – 20 мкг/мл. Другие соединения (G2, G3, G4, G5, G6, G7, G10) проявляют меньшую ингибирующую активность по отношению исследуемым штаммам Staphуlococcus aureus, МПК – от 40 мкг/мл и выше. Наиболее высокую антибактериальную активность по отношению к спорообразующим бактериям Bacillus subtilis выявлено для соединений (G1, G8) (МПК – 20 мкг/мл). Соединения (G2, G3, G4, G5, G6, G7, G9, G10) в отношении споровых бактерий проявляют невысокую бактериостатическую активность (МПК составляют от 80 мкг/мл до 320 мкг/мл).
Таблица 1
Минимальная подавляющая концентрация 3–арилиминометилхромонов
|
Шифр соединения |
Минимальная подавляющая концентрация соединения, мкг/мл |
||||
|
St. aureus 209p |
St.aureus (Макаров) |
B. subtilis L-2 |
E. coli F–50 |
Ps. aeruginosa 9027 |
|
|
G1 |
20 |
20 |
20 |
80 |
>320 |
|
G2 |
40 |
320 |
320 |
40 |
>320 |
|
G 3 |
80 |
80 |
160 |
80 |
>320 |
|
G4 |
80 |
40 |
80 |
160 |
>320 |
|
G5 |
40 |
40 |
80 |
160 |
>320 |
|
G6 |
40 |
40 |
80 |
80 |
>320 |
|
G7 |
160 |
80 |
160 |
80 |
>320 |
|
G8 |
10 |
10 |
20 |
40 |
>320 |
|
G9 |
20 |
20 |
160 |
40 |
>320 |
|
G10 |
80 |
40 |
160 |
160 |
>320 |
|
Норсульфазол |
40 |
40 |
40 |
40 |
Не активен |
3–арилиминометилхромоны проявляют невысокую бактериостатическую активность в отношении грамотрицательных бактерий E.coli F–50 (МПК составляет от 80 мкг/мл до 320 мкг/мл) и Ps.aeruginosa 9027 (МПК – выше 320 мкг/мл). Соединения (G2, G8, G9) губительно действуют в отношении штамма E.coli (МПК составляет 40 мкг/мл).
Представленные данные свидетельствуют о том, что высокое бактериостатическое действие 3–арилиминометилхромонов (G1, G8, G9) в отношении штаммов грамположительных бактерий: Staphуlococcus aureus и Bacillus subtilis, штамма грамотрицательных бактерий: Escherichia coli, обусловлено содержанием в их структуре нескольких фармакофорных групп. Соединения (G8, G9), содержащее электронодонорную группу (ацетоксигруппа) в положении 7 хромонового кольца (кольцо А), проявляют наибольшую бактериостатическую активность по отношению к штаммам Staphуlococcus aureus, Bacillus subtilis, Escherichia coli, что обусловлено формированием единой цепи сопряжения за счет стабилизацией плоскостной ориентации кольца «А», достигаемое за счет удлинения внутренней цепи сопряжения. Введение брома в положение 4´ фрагмента В существенно усиливает антибактериальную активность (антистафилакокковую активность).
ЗАКЛЮЧЕНИЕ
Таким образом, установлено, что 3–арилиминометилхромоны активнее антибактериального препарата из группы сульфаниламидов – норсульфазола по отношению к болезнетворным штаммам Staphуlococcus aureus, Bacillus subtilis, Escherichia coli. Невысокую бактериостатическую активность синтезированные соединения проявляют по отношению к штамму Pseudomonas aeruginosa. Экспериментальные исследования показали, что природа и положение заместителей в структуре 3-арилиминометилхромонов влияет на их антибактериальную активность в отношении штаммов Staphуlococcus aureus, Bacillus subtilis, Escherichia coli.
REFERENCES
- Supotnitsky M. V. Mechanisms for the development of antibiotic resistance in bacteria, Biological products, 2, 4 (2011).
- Khaeva O. E. Synthesis and electrochemical reactions of pharmacologically active derivatives of benz-γ-pyrone, abstract … candidate of chemical sciences, 21 (2001).
- Ikoeva L. P., Khaeva O. E., Lyutkin N. I. 7-Acetoxy-3-(N-bromophenyl)-iminomethylchromone, possessing antibacterial activity, Pat. 2186777 Ros. Federation IPC51 C07D311 / 22, A61K31 / 352, A61P31 / 04/ Ikoeva L. P., Khaeva O. E., Lyutkin N. I.; Applicant and patent holder North Caucasian Research Institute of Mining and Piedmont Agriculture. – No. 2000131803/04; application 12/18/2000; publ. 08/10/2002, Bull. Number 22.
- Khaeva O. E., Tsaliev A. B. 4-Iminomethyl-3-(7-acetoxychromon-3-yl)-benzoic acid, which has antibacterial activity, Pat. 2404174 ROS. Federation IPC51 C07D 311/22, A61K 31/352, A61P 31/04. / Khaeva O. E., Tsaliev A. B. – No. 2008148425/04; declared 12/08/2008; publ. 11/20/2010, Bull. Number 32.
- Vedmina E. A., Furer N. M. Guide to microbiology, clinic and epidemiology of infectious diseases, publ. of the Medicine, 1, 670 (1964).
- Pershin G. N. Methods of experimental chemotherapy, publ. of the Medicine, 530 (1971).



