NICKEL(II) COMPLEX WITH AZOMETHINE DERIVATIVE OF 4-FORMYL-3-METHYL-1-PHENYLPYRAZOL-5-ONE AND 2-FLUOROANILINE
КООРДИНАЦИОННОЕ СОЕДИНЕНИЕ НИКЕЛЯ(II) С АЗОМЕТИНОВЫМ ПРОИЗВОДНЫМ 3-МЕТИЛ-1-ФЕНИЛ-4-ФОРМИЛПИРАЗОЛ-5-ОНА И 2-ФТОРАНИЛИНА
JOURNAL: «SCIENTIFIC NOTES OF V.I. VERNADSKY CRIMEAN FEDERAL UNIVERSITY. Biology. Chemistry» Volume 10 (76), №1, 2024
Publication text (PDF): Download
UDK: 546.742:547.775:543.442.3
AUTHOR AND PUBLICATION INFORMATION
AUTHORS:
Baluda Yu. I., FRC for problems of chemical physics and medicinal chemistry of RAS, Chernogolovka, Russia
Gusev A. N., V. I. Vernadsky Crimean Federal University, Simferopol, Russia
Shulgin V. F., V. I. Vernadsky Crimean Federal University, Simferopol, Russia
Kryukova M. A., Saint Petersburg State University, Saint Petersburg, Russia
TYPE:Article
DOI:https://doi.org/10.29039/2413-1725-2024-10-1-276-284
PAGES:from 276 to 284
STATUS:Published
LANGUAGE:Russian
KEYWORDS: nickel, Schiff bases, 4-formyl-3-methyl-1-phenylpyrazol-5-one, X-ray diffraction study.
ABSTRACT (ENGLISH):
The synthesis, characterization and X-ray study of a new azomethine-based Ni(II) complex are described in present work. The Schiff base ligand HL was prepared by condensation of 4-formyl-3-methyl-1-phenylpyrazol-5-one and 2-fluoroaniline in ethanol medium. The target coordination compound was synthesized by reaction of HL and nickel(II) acetate tetrahydrate (2:1) in acetonitrilic solution using triethylamine as a base.
A comparative analysis of the IR-spectra showed that the ligand coordination is accompanied by its transition from the keto-enamine form to the imino-enol one, as evidenced by the disappearance of an absorption band with a maximum at 1658 cm-1, which is characteristic for the pyrazol-5-ones keto group, and a band with a maximum at 1287 cm-1, which is typical for C–N bonds of secondary amines. A narrow band with a maximum at 3619 cm-1, observed in complex spectra, indicates the coordination of water molecules, since this band shape is characteristic for vibrations of isolated molecules.
According to X-ray study results, a mononuclear discrete molecular complex [Ni(H2O)2L2] is formed. The coordination number of the nickel ion is 6, and its environment is a slightly distorted octahedron. The ligand is deprotonated and coordinated in imino-enol form. The water molecules are coordinated in the cis-position. It was found that coordinated water molecules and pyrazole nitrogen atoms of ligands are involved in the formation of hydrogen bonds. This leads to the assembling of complex particles into the linear one-dimensional supramolecular structure in the crystalline state. The distance between nickel ions in the chain reaches 7.987 Ǻ.
ВВЕДЕНИЕ
Основания Шиффа – широко применяемый в координационной химии класс лигандов [1]. Достоинствами этих соединений являются доступность их предшественников, простота синтеза, широкие возможности для модификации структуры. Последнее особенно важно, поскольку дает возможность варьируя количество и топологию хелатирующих групп, вводя заместители с различными свойствами, используя стерические эффекты задавать структуру конечных комплексов. В свою очередь, геометрия координационного полиэдра, ядерность, супрамолекулярная организация координационных соединений являются определяющими факторами для проявления тех или иных значимых свойств [2–6]. В частности, особенно сильно эти факторы сказываются на магнитных свойствах соединений, в том числе молекулярно-магнитных [7]. Ранее в рамках нашей работы были получены и исследованы с точки зрения структуры и магнитных свойств ряд комплексов Ni2+ кубанового типа с тридентатным азометиновым лигандом на основе 3-метил-1-фенил-4-формилпиразол-5-она и 2-аминофенола [8], а также моноядерные комплексы Ni2+ и Co3+ с аналогичным лигандом на основе 4-бензоил-3-метил-1-фенилпиразол-5-она [9]. В продолжение этой серии логичным было исследовать координацию ионов 3d-металлов с бидентатными лигандами такого типа, для чего использовать в качестве аминного компонента производные анилина, не содержащие дополнительных донорных атомов.
МАТЕРИАЛЫ И МЕТОДЫ
Синтез лиганда HL. К 0,605 г (3 ммоль) 3-метил-1-фенил-4-формилпиразол-5-она (получен согласно [10]), растворенного в 15 мл кипящего этанола, прибавили при перемешивании 0,335 г (3 ммоль) 2-фторанилина в 5 мл этанола. Раствор продолжили перемешивать при кипении с обратным холодильником, и через 30 минут выпал обильный желтый кристаллический осадок. Спустя еще 1,5 часа смесь упарили до 2–3 мл, охладили, отфильтровали; кристаллы промыли на фильтре небольшим количеством холодного этанола, высушили на воздухе. Получено 0,830 г вещества HL (2.81 ммоль), выход 94 %.
Найдено, %: C – 69,22; %: H – 4,49; N – 14,47. Для состава C17H14FN3O вычислено, %: C – 69,14; %: H – 4,78; N – 14,23.
ИК-спектр (νмакс, см-1): 1658 (с), 1626 (с), 1593 (ср), 1583 (ср), 1549 (ср), 1522 (ср), 1498 (ср), 1470 (ср), 1416 (сл), 1366 (ср), 1353 (ср), 1325 (ср), 1287 (с), 1234 (с), 1186 (с), 1097 (ср), 1049 (ср), 1007 (ср), 952 (ср), 905 (сл), 840 (сл), 799 (ср), 748 (оч.с), 690 (с), 666 (с), 580 (с), 507 (ср), 495(ср), 424 (ср).
Синтез комплекса [Ni(H2O)2L2]. К 0,295 г (1 ммоль) лиганда HL, растворенного в 20 мл кипящего ацетонитрила, прибавляли 0,125 г (0.5 ммоль) ацетата никеля(II) тетрагидрата и 0,139 мл триэтиламина (0,101 г, 1 ммоль). Раствор, изначально желтого цвета, менял окраску на салатовую. Смесь перемешивали при кипении 15 минут, упарив приблизительно до 10 мл, затем отфильтровали горячей и оставили для кристаллизации. В течение нескольких часов из раствора выпадали зеленые кристаллы ромбической формы, пригодные для РСА.
Найдено, %: C – 60,07; %: H – 4,36; N – 12,21. Для состава C34H30F2N6NiO4 вычислено, %: C – 59,76; %: H – 4,43; N – 12,30.
ИК-спектр (νмакс, см-1): 3619 (сл), 1626 (ср), 1595 (ср), 1586 (ср), 1531 (ср), 1493 (с), 1456 (ср), 1393 (сл), 1354 (ср), 1339 (ср), 1238 (ср), 1187 (ср), 1098 (сл), 1064 (сл), 1029 (сл), 1000 (сл), 970 (сл), 924 (сл), 854 (сл), 818 (ср), 750 (с), 693 (ср), 676 (ср), 625 (ср), 585 (ср), 556 (ср), 510 (ср), 494 (ср), 440 (ср).
Элементный анализ выполнен на автоматическом CHN-анализаторе Euro Vectоr EuroEA 3000. ИК-спектры записаны на ИК-спектрометре с Фурье-преобразованием Perkin Elmer Spectrum Two, снабженном приставкой НПВО, в диапазоне 4000 – 400 см-1. Спектры диффузного отражения поликристаллических образцов в УФ- и видимом диапазонах регистрировали на спектрофотометре Cintra 4040. Термогравиметрические исследования проводили на синхронном термическом анализаторе Perkin Elmer STA 6000 в атмосфере азота, скорость нагрева 10 °С/мин.
Рентгеноструктурный анализ монокристаллов комплекса проводился на дифрактометре Agilent Technologies SuperNova, оснащенном детектором HyPix3000, при температуре 100 K с использованием монохроматического CuKα излучения (λ=1,54184 Å) по стандартной процедуре; введена поправка на поглощение с использованием сферических гармоник. Структура расшифрована прямым методом и уточнена с помощью программы SHELXL 2014/7, встроенной в программный пакет OLEX2 в полноматричном анизотропном приближении для всех неводородных атомов [11, 12]. Атомы водорода генерированы геометрически и уточнены в модели наездника.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Органический лиганд и комплекс никеля на его основе были охарактеризованы методом ИК-спектроскопии. Известно, что для азометиновых производных
4-ацилпиразол-5-онов возможно существование четырех таутомерных форм, и преобладающей является кето-енаминная (рис. 1) [13]. Сравнительный анализ спектров показал, что при координации данного лиганда происходит его переход из кето-енаминной формы в имино-енольную, о чем свидетельствует исчезновение интенсивной полосы поглощения с максимумом при 1658 см-1, характерной для кетогруппы пиразол-5-онов, и сильной полосы с максимумом при 1287 см-1, типичной для связи C–N вторичных аминов. Однозначно идентифицировать появление в спектре комплекса сигналов колебаний связей C=N (в области 1630–1590 см-1) и С–О (в области 1370–1330 см-1) сложно ввиду наложения полос. В то же время, в спектре комплекса отчетливо наблюдается узкая полоса с максимумом при 3619 см-1, которая с высокой вероятностью указывает на координацию металлом молекул воды, т.к. такая форма полосы характерна для колебаний О–Н именно изолированных молекул.
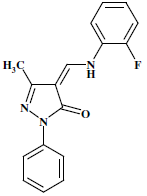
Рис. 1. Строение лиганда HL.
В спектре электронного поглощения твердого образца комплекса регистрируется широкая полоса при 663 нм, которая может быть отнесена к спин-разрешённому d–d переходу 3T1g(F)←3A2g. Другая более слабая широкая полоса, которая сосредоточена при 997 нм, может быть отнесена к переходу 3T2g←3A2g. Эти значения согласуются с литературными значениями для октаэдрических соединений Ni(II) соединений. В ближней УФ-области регистрируется интенсивная полоса с максимум при 376 нм, относящаяся к n–π* переходу лиганда.
Комплекс термически устойчив до температуры 108 оС, по достижении которой начинается удаление двух координированных молекул воды (6,1 % найдено / 5,3 % рассчитано). Процесс дегидратации продолжается до 150 оС и сопровождается мощным эндотермическим эффектом с максимумом при 138 оС. В интервале температур 150–290 оС масса образца остается постоянной, однако эндотермический эффект с максимумом при 258 оС указывает на реализацию фазового перехода. При температуре выше 300 оС начинается быстрая деградация комплекса, заканчивающаяся при температуре выше 780 оС образованием оксида никеля(II).
Для объективного установления кристаллической структуры координационного соединения был выполнен РСА монокристаллов. Основные сведения об эксперименте приведены в табл. 1. Согласно его результатам, формируется моноядерный дискретный молекулярный комплекс [Ni(H2O)2L2]. Координационное число иона никеля равно 6, а его окружение представляет собой слабо искаженный октаэдр. Лиганд депротонирован и координируется в имино-енольной форме. Молекулы воды координированы в цис-положении. Значения характерных длин связей и валентных углов в структуре комплекса приведены в табл. 2.
На рис. 2 представлено молекулярное строение исследуемого комплекса. Связи Ni–O несколько длиннее в случае атомов кислорода воды (менее чем на 0,1 Ǻ) по сравнению с таковыми для енольной группы азометина; длины связей Ni-N имеют промежуточное значение. Валентные углы в структуре координационного полиэдра незначительно деформированы – в пределах 5° в случае прямых углов и 10° в случае развернутых; помимо этого, присутствует небольшая асимметрия, выражающаяся в различии величин валентных углов N1–Ni1–O1 и O1–Ni1–O2 в зависимости от того, к какой из двух молекул лиганда принадлежит атом О1. Ион металла незначительно смещен относительно хелатных циклов: плоскости O1-Ni1-N1 и плоскости циклов образуют торсионные углы, равные 11,83° и 13,09°. Фторфенильные заместители развернуты относительно хелатных циклов на 68,75°. Атомы фтора в структуре заместителей несколько разупорядочены по двум
о-положениям. Межатомные расстояния Ni…F равны 3,632 Ǻ.
Обнаружено, что координированные молекулы воды и пиразольные атомы азота (N3) лигандов участвуют в образовании системы водородных связей. Это приводит к формированию в кристаллическом состоянии супрамолекулярной структуры линейного типа (рис. 3). Расстояние между ионами никеля в цепи составляет 7,987 Ǻ. Значения параметров водородной связи – расстояний О–Н (0,923 Ǻ), N…H (1,889 Ǻ), N…O (2,811 Ǻ), угла N–H–O (177,05°) свидетельствуют о том, что данная связь является весьма прочной [14].
Таблица 1.
Кристаллографические данные и параметры уточнения
кристаллической структуры комплекса 1.
| Параметр | Значение |
| Брутто-формула | C34H30F2N6NiO4 |
| М, г/моль | 683.35 |
| Сингония | моноклинная |
| Пространственная группа | С 2/с |
| a, Å | 13.1971 |
| b, Å | 15.5930 |
| c, Å | 15.9710 |
| α, ° | 90 |
| β, ° | 111.228 |
| γ, ° | 90 |
| Объем ячейки, Å3 | 3063.55 |
| Z | 4 |
| ρcalc, г/см3 | 1.482 |
| μ, мм‑1 | 1.448 |
| F(000) | 1416 |
| Θ, ° | 4.565 – 76.875 |
| Всего рефлексов | 3170 |
| Независимых рефлексов | 3021 |
| Рефлексы/ограничения/число уточняемых параметров | 3170/0/229 |
| GOOF | 1.041 |
| R1, % | 3.06 |
Таблица 2.
Длины связей и валентные углы в структуре координационного полиэдра.
| Параметр | Значение | Параметр | Значение |
| Ni1–O1, Ǻ | 2.027 | N1–Ni1–O2 (цис-),° | 91.48 |
| Ni1–O2, Ǻ | 2.112 | N1–Ni1–O2 (транс-),° | 176.63 |
| Ni1–N1, Ǻ | 2.089 | O1–Ni1–O1,° | 172.29 |
| N1–Ni1–N1,° | 91.80 | O1–Ni1–O2,° | 85.70/88.63 |
| N1–Ni1–O1,° | 91.97/93.40 | O2–Ni1–O2,° | 85.26 |
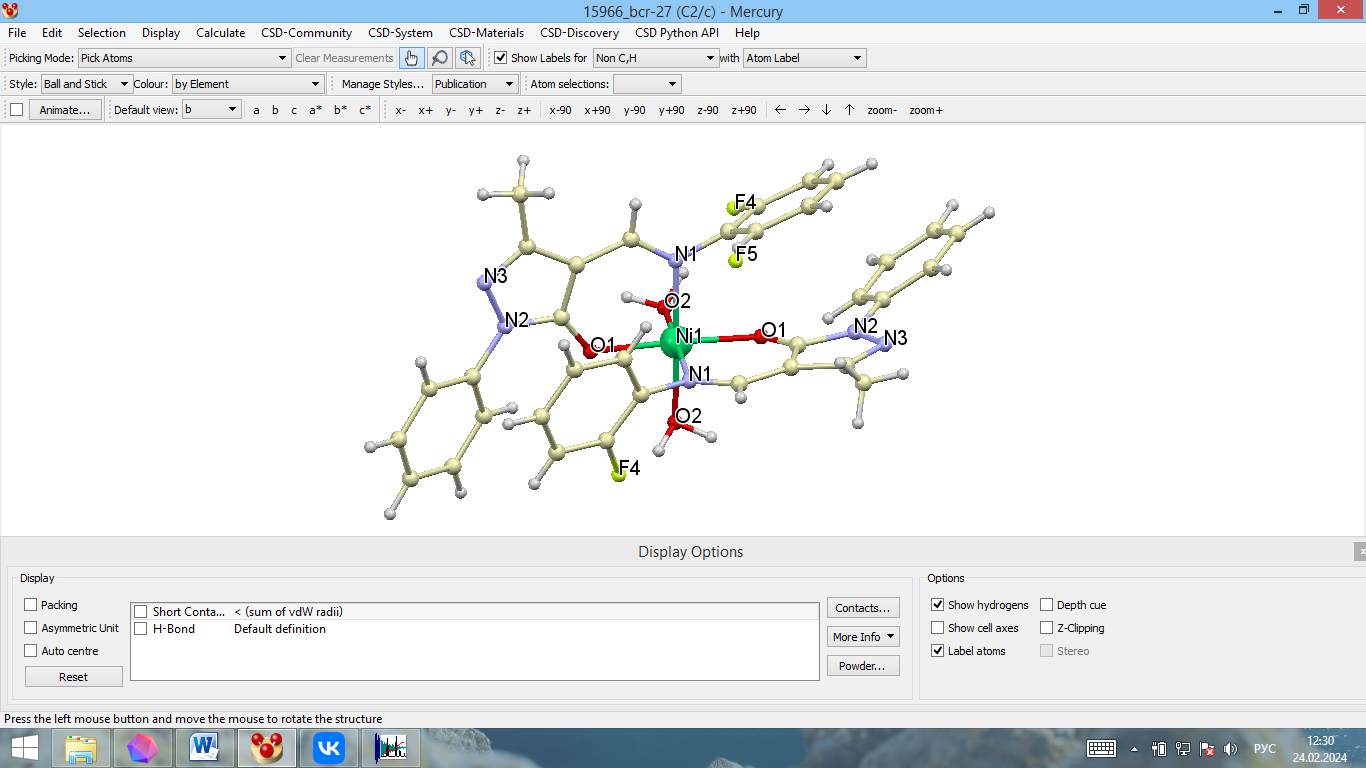
Рис. 2. Молекулярная структура комплекса [Ni(H2O)2L2].
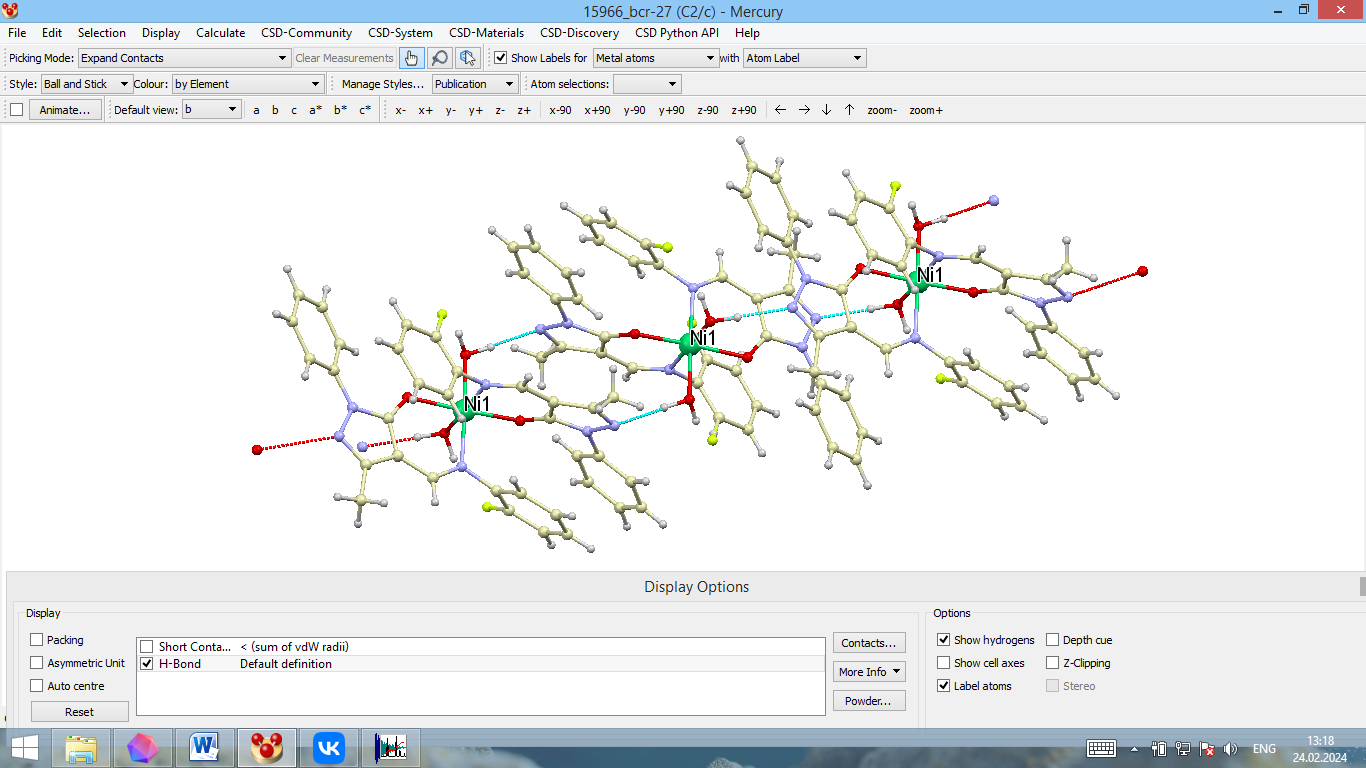
Рис. 3. Образование линейной цепи посредством водородных связей.
ЗАКЛЮЧЕНИЕ
В рамках проведенного исследования получен комплекс никеля с основанием Шиффа – производным 3-метил-1-фенил-4-формилпиразол-5-она и 2-фторанилина. Установлено образование нейтрального комплекса состава [Ni(H2O)2L2]. Ион никеля гексакоординирован и обладает геометрией окружения, близкой к правильной октаэдрической. Молекулы воды координируются в цис-положении. Взаимодействие комплексных частиц посредством водородных связей приводит к образованию супрамолекулярной 1-D структуры.
- Boulechfar C., Ferkous H., Delimi A., Djedouani A., Kahlouche A., Boublia A., Darwish A. S., Lemaoui T., Verma R., and Benguerba Y. Schiff bases and their metal complexes: a review on the history, synthesis, and applications. Inorg. Chem. Comm., 150, 110451 (2023).
- Böhme M., Ziegenbalg S., Aliabadi A., Schnegg A., Görls H., and Plass W. Magnetic relaxation in cobalt(II)-based single-ion magnets influenced by distortion of the pseudotetrahedral [N2O2] coordination environment. Dalton Trans., 47, 10861 (2018).
- Ziegenbalg S., Hornig D., Görls H., and Plass W. Сobalt(II)-based single-ion magnets with distorted pseudotetrahedral [N2O2] coordination: experimental and theoretical investigations. Inorg. Chem., 55 (8), 4047 (2016).
- Peng G., Chen Yu., Li B., Zhang Y.-Q., and Ren X.-M. Bulky Schiff-base ligand supported Co(II) single-ion magnets with zero-field slow magnetic relaxation. Dalton Trans., 49, 5798 (2020).
- Liang L., Li W., Sun Ya., Li M., Xu X., Wu T., and Xie Sh. A cuboidal tetranuclear nickel cluster based on O,O,N-tridentate Schiff base: synthesis, structure and magnetic properties. J. Clust. Sci., 29, 151 (2018).
- Herchel R., Nemec I., Machata M., and Trávníček Z. Solvent-induced structural diversity in tetranuclear Ni(II) Schiff-base complexes: the first Ni4 single-molecule magnet with a defective dicubane-like topology. Dalton Trans., 45, 18622 (2016).
- Ungur L., Chibotaru L. F. Strategies toward high-temperature lanthanide-based single-molecule magnets. Inorg. Chem., 55, 10043 (2016).
- Gusev A. N., Nemec I., Herchel R., Baluda Yu. I., Kryukova M. A., Efimov N. N., Kiskin M. A., and Linert W. A new series of Schiff base Ni(II)4 cubanes: evaluation of magnetic coupling via carboxylate bridges. Polyhedron, 196, 115017 (2021).
- Gusev A. N., Baluda Y. I., Shulgin V. F., Kryukova M. A., and Kiskin M. A. 4-Benzoyl-3-methyl-1-phenylpyrazol-5-one based complexes of nickel(II) and cobalt(III) with a Schiff base. J. Struct. Chem., 64 (11), 2090 (2023).
- Jensen B. S. The synthesis of 1-phenyl-3-methyl-4-acyl-pyrazolones-5. Acta Chem. Scand., 13 (8), 1668 (1959).
- Dolomanov O. V., Bourhis L. J., Gildea R. J., Howard J. A. K., and Puschmann H. OLEX2: a complete structure solution, refinement and analysis program. J. Appl. Crystallogr., 42, 339 (2009).
- Sheldrick G. M. Crystal structure refinement with SHELXL. Acta Crystallogr. Sect. C Struct. Chem., 17, 3 (2015).
- Marchetti F., Pettinari C., Di Nicola C., Tombesi A., and Pettinari R. Coordination chemistry of pyrazolone-based ligands and applications of their metal complexes. Coord. Chem. Rev., 401, 213069 (2019).
- Steed J. W., Atwood J. L. Supramolecular Chemistry 2nd ed. Chichester, John Wiley & Sons Ltd., 998 p. (2009), ISBN: 978-1-118-68150-3.



