SYNTHESIS OF NANOSIZED YTTRIUM ALUMINUM GARNET POWDERS USING ION-EXCHANGE RESIN
СИНТЕЗ НАНОРАЗМЕРНЫХ ПОРОШКОВ АЛЮМОИТТРИЕВОГО ГРАНАТА С ИСПОЛЬЗОВАНИЕМ ИОНООБМЕННОЙ СМОЛЫ
JOURNAL: «SCIENTIFIC NOTES OF V.I. VERNADSKY CRIMEAN FEDERAL UNIVERSITY. Biology. Chemistry» Volume 10 (76), №1, 2024
Publication text (PDF): Download
UDK: 546.05
AUTHOR AND PUBLICATION INFORMATION
AUTHORS:
Shergin A. V., Chelyabinsk State University, Chelyabinsk, Russia
Belaya E. A., Chelyabinsk State University, Chelyabinsk, Russia
Zherebtsov D. A., South Ural State University, Chelyabinsk, Russia
TYPE:Article
DOI:https://doi.org/10.29039/2413-1725-2024-10-1-307-315
PAGES:from 307 to 315
STATUS:Published
LANGUAGE:Russian
KEYWORDS: YAG, ion-exchange synthesis, scanning electron microscopy, X-ray phase analysis.
ABSTRACT (ENGLISH):
The article presents the synthesis of nanosized powders of yttrium aluminum garnet Y3Al5O12 using a KU-2 8 chS cation-exchange resin. It is shown that in the volume of the granules of this resin, the cation exchange of H+ ions for Y3+ and Al3+ ions are possible, taking into account their different selectivity with respect to the cation exchanger, and a homogeneous distribution of both cations in the mass of the ion exchange resin is achieved. It has been established that subsequent washing, drying of the obtained material for 12 hours and heat treatment in air in a muffle furnace at 1000℃ for 3 hours leads to the formation of a monophase sample of yttrium aluminum garnet. The resulting product was a white powder, which was examined by X-ray phase analysis and scanning electron microscopy. X-ray phase analysis confirmed that the final product has a garnet structure with the Ia3d symmetry space group. The resulting sample does not contain foreign phases in the form of intermediate compounds or initial components of the reaction. The set of diffraction maxima made it possible to calculate the main characteristics of the structure: the unit cell parameter a, the unit cell volume V, and the width of the coherent scattering region. The reliability of the calculations is confirmed by the values of the profile (Rp) and weighted (Rwp) convergence factors, which were less than 12 %. The value of the size of the coherent scattering region calculated using the Williamson-Hall equation was 19 nm. According to the data of scanning electron microscopy, the sample is a spherical particle with a diameter of about 15–30 nm, which agrees with the width of the coherent scattering region. Nanoparticles are folded into porous aggregates having multimicron sizes.
ВВЕДЕНИЕ
В настоящее время порошок алюмоиттриевого граната Y3Al5O12 (ИАГ/YAG) не находит широкого применения в чистом виде. Допирование ионами Ce3+ приводит к появлению люминесцентных свойств, благодаря чему такой материал находит широкое применение в качестве люминофорного конвертера для светодиодных искусственных источников освещения [1–5]. Допирование ИАГ ионами Nd3+ приводит к появлению люминесценции в ближней ИК области, что применяется как в лазерах с диодной накачкой [6–8], так и в качестве сцинтилляторов в медицинской радиационной дозиметрии [9, 10]. В настоящее время синтезируют алюмоиттриевый гранат различными методами, но самым распространенным до сих пор является твердофазный или керамический [11–15]. Основными недостатками этого метода являются низкая начальная степень гомогенизации шихты, что приводит к необходимости использования высоких температур термообработки (выше 1300 °С), что повышает степень агломерации частиц, а также необходимость в использовании сверхчистых оксидов иттрия и алюминия в качестве исходного сырья. В последнее время чаще используется золь-гель метод, который позволяет снизить температуру образования чистой фазы алюмоиттриевого граната до 900 °С, обеспечивает хорошее смешивание исходных материалов и хорошую химическую однородность продуктов. Гомогенность геля намного выше, чем у аналогичных смесей оксидов, приготовленных для твердофазного спекания [16, 17]. Однако ультрамелкие частицы гелеобразного продукта подвергаются сильной агломерации во время термообработки, что приводит к плохой спекаемости полученных порошков. А также золь-гель метод требует значительных объемов растворов и соответствующих аппаратов. В связи с этим разработка альтернативных способов синтеза порошков алюмоиттриевого граната является актуальной задачей.
В данной работе представлена методика синтеза наноразмерных порошков алюмоиттриевого граната с применением катионообменной смолы марки КУ-2 8 чС. Неоспоримым преимуществом ионообменного синтеза перед керамическим является повышение дисперсности и гомогенизации компонентов, а также невысокие температуры термообработки.
Сущность предложенного метода синтеза состоит в избирательной адсорбции катионов металлов в объеме катионита, что отражено в рядах селективности [18]:
Li+ < Na+ <К+ < Rb+ < Cs+
Mg2+ < Ca2+ < Sr2+ < Ba2+
Изменение энергии гидратации ионов при их переходе из водного раствора в фазу ионита является определяющим в их расположении в рядах селективности. Энергия гидратации уменьшается с увеличением радиусов ионов, следовательно, селективность катионита к катионам закономерно возрастает с увеличением их размеров. Ионный радиус катионов Y3+ и Al3+, составляющих алюмоиттриевый гранат составляет 0,92 и 0,39 Å соответственно [19]. Переход более селективно сорбируемого из внешнего раствора в фазу ионита требует меньших энергетических затрат на частичную дегидратацию иона и приводит к наибольшему выделению энергии при его взаимодействии с функциональной группой. Напротив, перемещение менее селективно сорбируемого и более гидратированного иона из ионита в раствор связано с меньшими затратами энергии на преодоление электростатического взаимодействия с функциональной группой и сопровождается выделением энергии вследствие дополнительной гидратации этого иона в растворе.
Катионообменная смола, находящаяся в H+–форме, представляет собой полимер с функциональными группами –SO3H, в которых протоны способны замещаться на катионы Y3+ и Al3+. Общую схему процесса ионообменного синтеза можно представить следующим образом:
| R–SO3H + Y3+/Al3+ → (R–SO3)3Y3+/Al3+ + 3H+ | (1) |
Катионообменная смола с адсорбированными на ней катионами подвергается термообработке, что приводит к полному окислению катионита и формированию из образовавшихся оксидов иттрия и алюминия ИАГ.
МАТЕРИАЛЫ И МЕТОДЫ
Для синтеза в качестве исходных компонентов использовали кристаллогидраты нитратов иттрия YNO3·6H2O и алюминия Al(NO3)3·9H2O, навески которых были взяты в стехиометрическом соотношении Y:Al=3:5. Далее каждый компонент отдельно растворили в 25 мл дистиллированной воды при постоянном перемешивании на магнитной мешалке. Затем 1 г катионообменной смолы поместили в раствор, содержащий ионы Y3+ на 1 час при постоянном перемешивании. Затем навеску катионита с адсорбированными ионами иттрия отфильтровали, промыли небольшим количеством дистиллированной воды от маточного раствора и поместили в химических стакан, содержащий ионы Al3+, на 15 минут при постоянном перемешивании. После этого, катионит с адсорбированными катионами алюминия и иттрия промыли дистиллированной водой от остатков раствора и высушили на воздухе при комнатной температуре в течение 12 часов. На последней стадии синтеза катионит подвергли термообработке в муфельной печи в воздушной атмосфере при температуре 1000°С в течение 3 часов.
Рентгенофазовый анализ (РФА) полученных образцов проводили на порошковом рентгеновском дифрактометре ДРОН-3М с излучением CuKα, с фокусировкой по Брэггу-Брентано, при температуре 298К, со скоростью съемки 2 град/мин. Для определения фазового состава образца была использована база данных JCPDS.
Уточнение структуры образцов проводили методом Ритвельда с использованием программного пакета JANA2006 [20]. Ширину области когерентного рассеяния (ОКР) рассчитывали по уравнению Вильямсона-Холла:
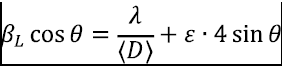 (2)
(2)
Морфологию поверхности и размеры частиц изучали с помощью сканирующего электронного микроскопа Jeol JSM-7001F при напряжении электронной пушки 20 кВ.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Условия ионообменного синтеза были подобраны исходя из того, что ион с большей селективностью способен замещать как свободные –SO3H группы, так и уже адсорбированные катионы металлов с меньшей селективностью, так как это связано с различными энергетическими затратами при переходе катиона из раствора в фазу ионита. Схема такого процесса:
| R–(SO3)3Al3+ + Y3+→ R–(SO3)3Y3+ + Al3+ | (3) |
Влияние последовательности адсорбции катионов при ионообменном синтезе было рассмотрено нами ранее в работе [21], где показано, что только такая схема синтеза приводит к получению монофазного образца ИАГ. Полученная дифрактограмма представлена на рис. 1, где все дифракционные максимумы соответствуют фазе ИАГ. В табл. 1 представлен набор дифракционных максимумов для исследуемого образца.
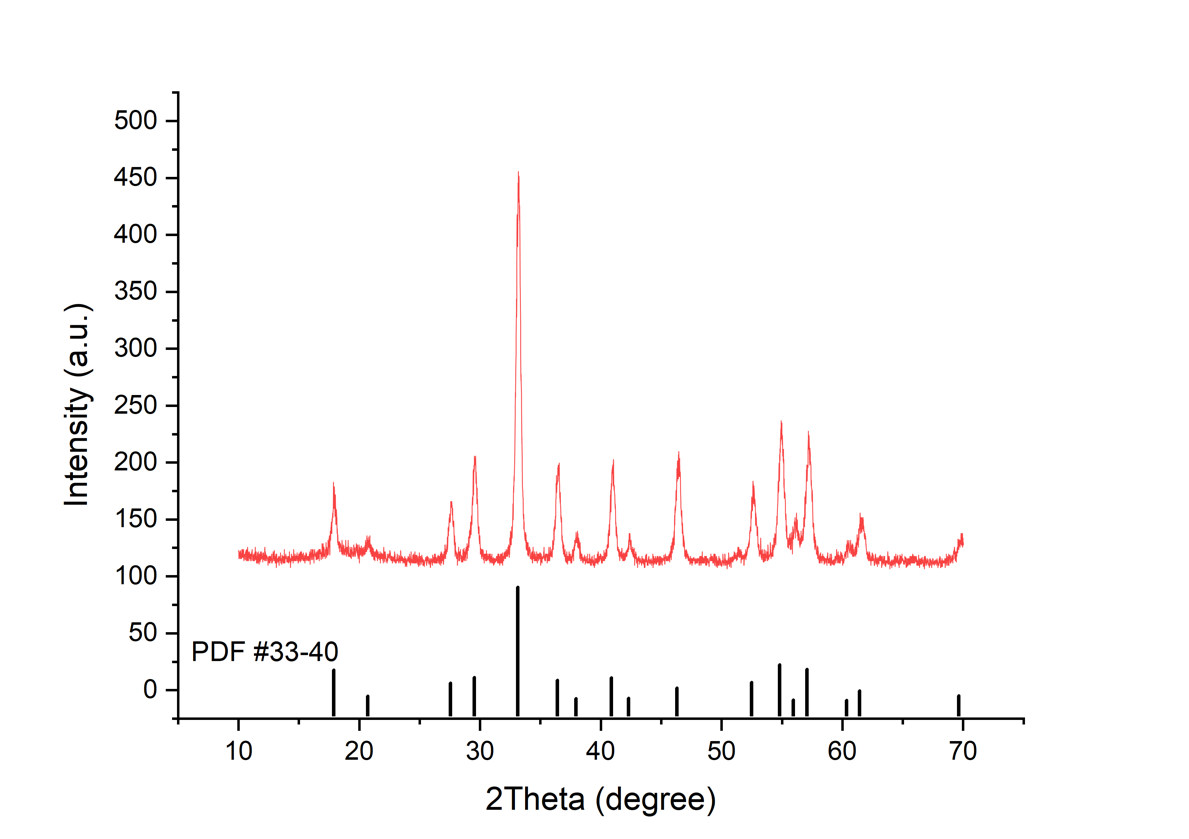
Рис. 1. Дифрактограмма образца алюмоиттриевого граната. Штрих диаграмма – карточка для Y3Al5O12 PDF №33-40.
Таблица 1
Набор дифракционных максимумов для образца алюмоиттриевого граната
| Угол дифракции 2θ, град | Межплоскостное расстояние d, Å | Относительная интенсивность I, % |
| 17,80 | 4,9828 | 18,29 |
| 20,76 | 4,2785 | 6,34 |
| 27,56 | 3,2364 | 19,02 |
| 29,62 | 3,0158 | 26,34 |
| 33,13 | 2,7039 | 100,00 |
| 36,45 | 2,4649 | 24,15 |
| 37,91 | 2,3732 | 7,56 |
| 40,89 | 2,2069 | 24,88 |
| 42,37 | 2,1332 | 7,80 |
| 46,41 | 1,9565 | 30,49 |
| 52,58 | 1,7405 | 20,00 |
| 55,00 | 1,6695 | 35,12 |
| 55,66 | 1,6513 | 6,59 |
| 57,14 | 1,6120 | 35,61 |
| 60,48 | 1,5307 | 4,63 |
| 61,51 | 1,5075 | 12,93 |
| 69,77 | 1,3479 | 5,85 |
Структуру полученного образца ИАГ уточняли методом Ритвельда. Теоретическую дифрактограмму построили, задав позиции атомов, начальное значение параметра элементарной ячейки алюмоиттриевого граната с пространственной группой симметрии Ia3d. Для описания формы дифракционных максимумов была использована аппроксимирующая функция Войта, представляющая собой линейную комбинацию функций Гаусса и Лоренца. Результаты уточнения представлены на рис. 2 и в табл. 2.
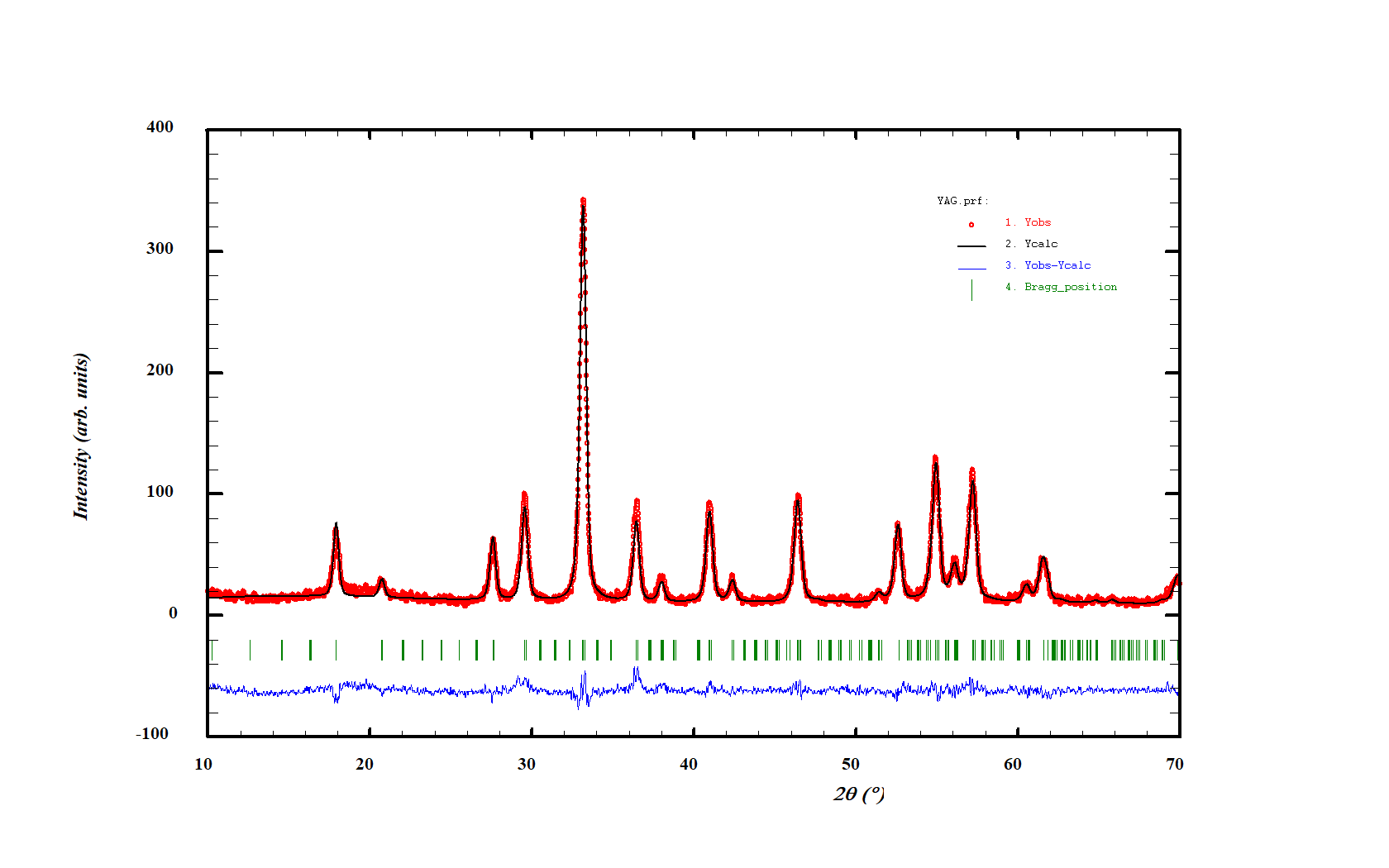
Рис. 2. Уточнение структуры образца YAG. Синяя линия – разница между экспериментом и расчетом.
Таблица 2
Результаты уточнения структуры
| Образец | Параметр решетки (а), Å | Объем решетки,Å3 | ОКР, нм | Факторы |
| PDF №33-40 | 12,006 | 1730,7 | – | – |
| YAG | 12,080±0,002 | 1776,9±0,3 | 19 | Rp = 8,81Rwp = 11,39 |
По данным проведенного анализа, учитывая значения профильного и взвешенного факторов Rp и Rwp, которые составили соответственно 8,81 % и 11,39 %, можно сделать вывод о том, что полученный образец кристаллизуется в решетке алюмоиттриевого граната с параметрами структуры, описанными выше. Размер ОКР составил 19 нм, что хорошо согласуется с данными сканирующей электронной микроскопии.
Морфология поверхности полученного образца показана на рис. 3.
 |
 |
| а | б |
Рис. 3. Электронно-микроскопические изображения поверхности образца алюмоиттриевого граната.
а) Увеличение x20,000 б) Увеличение х50,000.
Образец представляет собой частицы округлой формы, размером 15–30 нм в диаметре, большая часть из которых агрегирована в кластеры, размерами 1–2 мкм. Тенденция к образованию крупных агломератов, очевидно, связана с длительной термообработкой при температуре 1000 °С. Для понижения степени агломерации следует уменьшить время термообработки, а также уменьшить температуру, замедляя процесс диффузии. Однако при понижении температуры прокаливания, согласно фазовой диаграмме (рис. 4) возможно образование промежуточных соединений в виде моноклинной структуры YAlO3 и структуры перовскита Y4Al2O9.
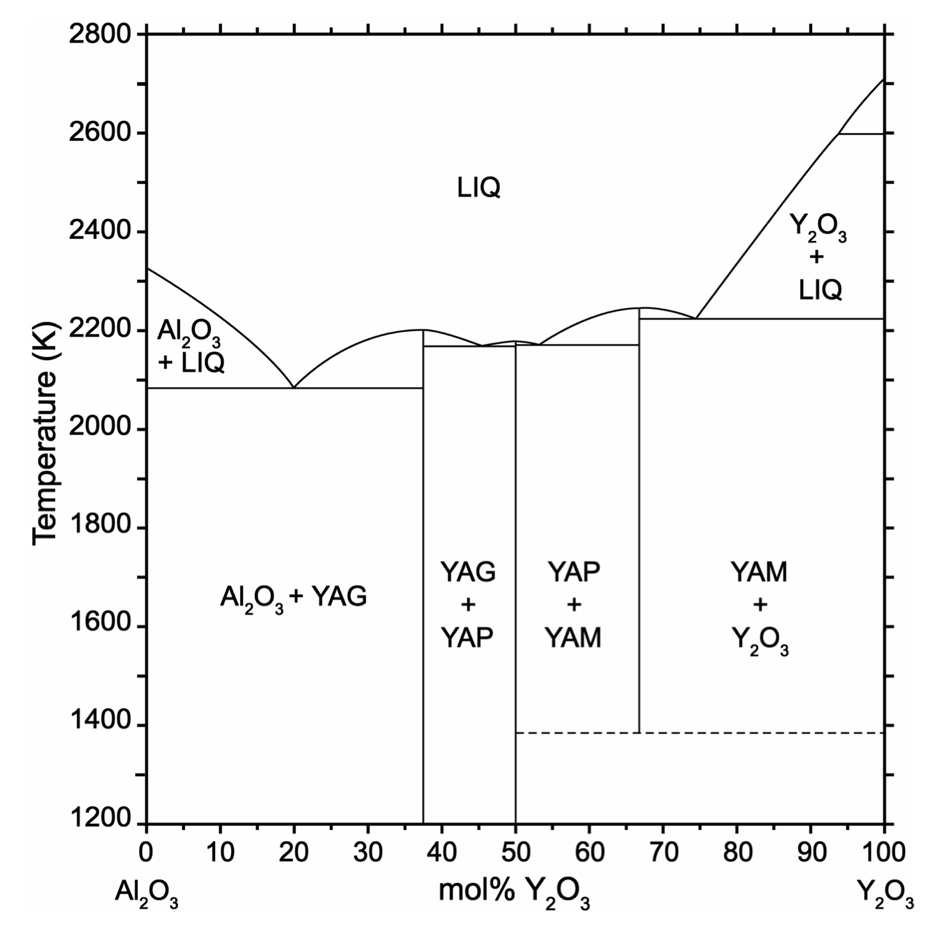
Рис. 4. Фазовая диаграмма двухкомпонентной системы Al2O3 – Y2O3 [22].
ЗАКЛЮЧЕНИЕ
Разработан метод синтеза порошка алюмоиттриевого граната на катионите марки КУ-2 8 чС. Согласно РФА, получен монофазный образец алюмоиттриевого граната, кристаллизующегося в пространственной группе Ia3d.
Методом Ритвельда уточнен параметр элементарной ячейки a и ее объем V, которые составили соответственно 12,080 Å и 1776,9 Å3. Значение факторов сходимости составило меньше 15%, что говорит о достоверности уточнения структуры.
Размер частиц по данным СЭМ варьирует в пределах 15–30 нм, что согласуется с вычисленной по уравнению Вильямсона-Холла шириной ОКР, составившей 19 нм. Наночастицы образуют агломераты размером 1–2 мкм, что может быть связано с длительной термообработкой при 1000°С.
- Nakamura S., Present performance of InGaN-based blue/green/yellow LEDs. Light-Emitting Diodes: Research, Manufacturing, and Applications, 3002, 26 (1997).
- Marin R., Sponchia G., Riello P., Sulcis R., Enrichi F., Photoluminescence properties of YAG: Ce3+, Pr3+ phosphors synthesized via the Pechini method for white LEDs. Journal of Nanoparticle Research, 14(6), 1 (2012).
- Xia Z., Meijerink A., Ce3+-Doped garnet phosphors: composition modification, luminescence properties and applications. Chemical Society Reviews, 46(1), 275 (2017).
- Nishiura S., Tanabe S., Fujioka K., Fujimoto Y., Properties of transparent Ce: YAG ceramic phosphors for white LED. Optical Materials, 33(5), 688 (2011).
- Asakura R., Isobe T., Kurokawa K., Aizawa H., Ohkubo M., Tagging of avidin immobilized beads with biotinylated YAG: Ce3+ nanocrystal phosphor. Analytical and bioanalytical chemistry, 386(6), 1641 (2006).
- Geusic J. E., Marcos H. M., Van Uitert L. G., Laser oscillations in Nd‐doped yttrium aluminum, yttrium gallium and gadolinium garnets. Applied Physics Letters, 4(3), 182 (1964).
- Benayas A., del Rosal B., Pérez-Delgado A., Santacruz-Gómez K., Jaque D., Hirata G.A.,
Vetrone F., Nd: YAG near‐infrared luminescent nanothermometers. Advanced Optical Materials, 3(5), 687 (2015). - Deineka T. G., Doroshenko A. G., Mateychenko P. V., Tolmachev A. V., Vovk E. A., Vovk O. M., Yavetskiy R. P., Baumer V. N., Sofronov D. S., Influence of sulfate ions on properties of co-precipitated Y3Al5O12: Nd3+ nanopowders. Journal of alloys and compounds, 508(1), 200 (2010).
- Sengar P., Borbón-Nuñezc H. A., Salas-Juárez Ch. J., Aguilar E. M., Cruz-Vázquez C.,
Bernal R., Hirata G. A., β-Irradiated thermoluminescence response of nanocrystalline YAG: Pr3+ for radiation dosimetry. Materials Research Bulletin, 90, 195 (2017). - Rivera T., Thermoluminescence in medical dosimetry. Applied radiation and isotopes, 71, 30 (2012).
- Xu S., Sun L., Zhang Y., Ju H., Zhao S., Deng D., Wang H., Wang B., Effect of fluxes on structure and luminescence properties of Y3Al5O12: Ce3+ phosphors. Journal of Rare Earths, 27(2), 327 (2009).
- Saat A., Hazimah H., Zaini H., Synthesis and characterization of YAG: Ce prepared by solid state reaction method. Malaysian Journal of Analytical Sciences, 15(1), 101 (2011).
- Huang S. C., Wu J. K., Hsu W. J., Chang H. H., Hung H. Y., Lin C. L., Su N. Bagkar W. C. Ke H. T. Kuo R. S., Liu R. S., Particle size effect on the packaging performance of YAG: Ce phosphors in white LEDs. International Journal of Applied Ceramic Technology, 6(4), 465 (2009).
- Chou C. S., Wu C. Y., Yeh C. H., Yang R. Y., Chen J. H. The optimum conditions for solid-state-prepared (Y3–xCex)Al5O12 phosphor using the Taguchi method. Advanced Powder Technology, 23(1), 97 (2012).
- Won C. W., Nersisyan H. H., Won H. I., Lee J. H., Lee K. H., Efficient solid-state route for the preparation of spherical YAG: Ce phosphor particles. Journal of Alloys and Compounds, 509(5), 2621 (2011).
- Hora D. A., Andrade A. B., Ferreira N. S., Teixeira V. C., Rezende M. V. D. S, Effect of the PVA (polyvinyl alcohol) concentration on the optical properties of Eu-doped YAG phosphors. Optical Materials, 60, 495 (2016).
- Su X., Zhou J., Bai G., Zhang J., Zhao P., Low temperature synthesis and characterization of YAG nanopowders by polyacrylamide gel method. Ceramics International, 42(15), 17497 (2016).
- Nesterov Yu. V., Ionites and ion exchange. Sorption technology for the extraction of uranium and other metals by underground leaching, 480 p. (Unicorn-izdat, 2007). (in Russ.).
- Batsanov S. S. Structural chemistry. Facts and dependencies, 292 p. (Dialogue-MSU, 2000). (in. Russ.).
- Petříček V., Dušek M., Palatinus L., Crystallographic computing system JANA2006: general features. Zeitschrift für Kristallographie-Crystalline Materials, 229(5), 345 (2014).
- Shergin A. V. Synthesis of yttrium aluminum garnet on an ion exchange matrix. Chemistry: Materials of the 60th International. scientific stud. conf. April 10–20, 2022, 218 (2022). (in. Russ.).
- Fabrichnaya O., Seifert H. J., Ludwig T., Aldinger F., Navrotsky A., The assessment of thermodynamic parameters in the Al2O3–Y2O3 system and phase relations in the Y–Al–O system. Scandinavian journal of metallurgy, 30(3), 175 (2001).

